
题目列表(包括答案和解析)
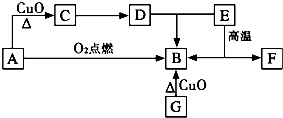 A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.?
A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.?A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1∶1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.
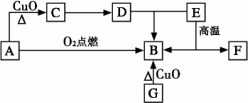
(1)D与E反应生成B的离子方程式:________.
(2)单质G中的元素位于第________周期________族.
G与F在高温下反应生成固体H和一种还原性气体,H与H2O反应生成可燃性气体I,I可通过两步反应制得A.请写出:
(3)I的结构式:________.
(4)由I制备A的两步反应的化学方程式:________,________.
(5)G与F在高温下反应生成固体H的化学反应方程式:________.
乙醇是日常生活中最常见的有机物之一,乙醇的一种工业制法如下:
乙烯+A CH3CH2OH
CH3CH2OH
请回答下列问题:
(1)反应物乙烯的电子式为
________________________________________________________________________;
已知该反应中原子利用率为100%,符合绿色化学思想,则反应物A的化学式为________________。
(2)工业上还可以用硫酸为吸收剂的间接水合法合成乙醇,从对设备的影响和产品分离角度分析该法与固体催化剂法相比,缺点是
________________________________________________________________________。
(3)乙酸和乙醇在一定条件下可发生反应生成一种有香味的物质,该反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
该反应是可逆反应,请说出提高反应物转化率的一种方法:
________________________________________________________________________。
(4)固体酒精是一种便携的燃料,其中一种制备方法是将饱和醋酸钙溶液加入酒精中致使醋酸钙从酒精溶液中析出,呈半固态的凝胶状物质——“胶冻”,酒精填充其中,点燃胶状物时,酒精便燃烧起来。该过程说明醋酸钙在酒精中的溶解度________(填“大于”或“小于”)醋酸钙在水中的溶解度。
| |||||||||||||||||||||||||||||
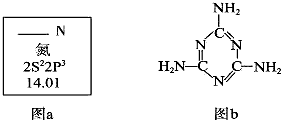
 则n值为_________。
则n值为_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com