
题目列表(包括答案和解析)
| ||
| ||
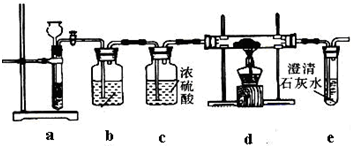
根据Mg与CO2的反应推测,Na也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种。某兴趣小组用如下装置开展两个阶段的实验探究。

【实验I】引发CO2与Na反应。操作步骤为:
①按图连接装置,检验装置气密性,并往各装置中加入试剂;
②打开装置a上活塞一段时间;
③点燃d处酒精灯,使CO2与Na充分反应。停止加热,继续通气体使双通管冷却。
回答下列问题:
(1)装置a中用到的玻璃仪器有试管和 ;
(2)装置b中装入的试剂是 ;
(3)装置c的作用是 ;
(4)步骤②中,当观察到 时,才能进入步骤③。
【实验Ⅱ】探究反应产物及反应机理。取反应后双通管中固体物质29.2 g进行如下实验:
①仔细观察固体,发现有黑色颗粒;
②将固体溶于足量的水并过滤、洗涤,得到1.8 g滤渣(干燥);
③将滤液加水稀释配成250 mL的溶液;
④取少量③的溶液,先加足量BaCl2溶液,观察到白色沉淀,所得固体质量为3.94g;再加几滴酚酞试液,溶液变红;
⑤取25.00 mL③的溶液,滴加甲基橙作为指示剂,用3.0 mol·L-1盐酸滴定,消耗盐酸体积为20.00 mL。
回答下列问题:
(5)如何判断⑤中的滴定终点
(6)反应后装置d中的固体物质为 ;通过计算分析:29.2 g残留固体中,各组分的质量各是多少?
(13分)根据镁与二氧化碳的反应推测,钠也能在二氧化碳中燃烧,且固体产物可能为碳酸钠、氧化钠、碳中的两种或三种。某兴趣小组用如下装置开展两个阶段的实验探究。

I、引发CO2与Na反应。操作步骤为:①按图连接装置,检验气密性,并往各装置中加入试剂;②打开装置a上活塞一段时间;③点燃d处酒精灯,使CO2与Na充分反应。停止加热,继续通气体使双通直管冷却。回答下列问题:
(1)操作①时,装置b中装入的试剂是 ;
(2)步骤②时,当观察到 时,才能进入步骤③。
Ⅱ:探究反应产物及反应机理。取反应后双通管中固体物质29.2g进行如下实验:
①仔细观察固体,发现有黑色颗粒;
②将固体溶于足量的水并过滤、洗涤,得到1.8 g滤渣(干燥);
③将滤液加水稀释配成250ml的溶液;
④取少量③的溶液,先加足量BaCl2溶液,再加酚酞试液,观察到白色沉淀及溶液变红;
⑤取25.0mL③的溶液,用3.0mol·L-1盐酸滴定,消耗盐酸20.00mL。回答下列问题:
(3)反应后装置d中的固体物质为
(4)通过计算分析:29.2g残留固体中,各组分的质量各是多少?
(5)该探究条件下,钠与二氧化碳反应的化学方程式为 。
(1)求混合物中Na2O2、Al的物质的量。________________
(2)将上述反应得到的溶液加入x mL 5.0mol/L的盐酸,充分反应后得到y g的沉淀。试确定x、y之间的关系。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com