
题目列表(包括答案和解析)
(1)Y元素的名称是___________________________________________:
(2)XZ3化合物的电子式是__________________________________;
(3)A、B、C的离子半径由大到小的顺序为________________________(用元素离子符号表示);
(4)化合物XZ4A中所含有的化学键类型为_______________________________________;
(5)元素组成为XZ5YC3和BCZ化合物反应的离子方程式为__________________________。
短周期的六种元素A、B、C、X、Y、Z,原子序数依次变小,其中X、Y、Z原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成10电子化合物Q;C与X处于同周期,B+与C2-的核外电子排布相同,A与B处于同周期,且形成BA型化合物。请回答:
(1)化合物Q的空间构型为_______________;化合物YC2电子式是________________;
(2)A、B、C的离子半径由大到小的顺序为____________________(用元素离子符号表示);
(3)元素组成为XZ5YC3和BCZ(足量)化合物反应的离子方程式为____________________;
(4)工业上,若输送元素A的单质的管道漏气,用Q进行检验时可观察到大量白烟,同时有X的单质生成,写出有关反应的化学方程式_______________________________________。
| 元素 | 信息 |
| B | 其单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性 |
| D | 其简单阳离子与X具有相同电子数,且是同周期中简单阳离子中半径最小的 |
| E | 元素原子最外层比次外层少2个电子 |
| C、F | 两种元素的原子最外层共有13个电子 |
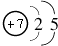
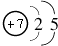
 Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH- Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-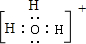
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com