
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
£¨13·Ö£©¢ñ£®ÏÂÁĐʵÑé²Ù×÷»̣ʵÑéĐđÊöƠưÈ·µÄÊÇ______________ £῭îĐ̣ºÅ£©
¢ÙÅäÖÆÂÈ»¯̀úÈÜ̉ºÊ±£¬Đè¼ÓÉÙÁ¿ÑÎË᣻
¢ÚÓĂ10 mLÁ¿Í²Á¿È¡5.80 mLÑÎË᣻
¢ÛÓĂÏ¡´×Ëá³ưÈ¥ÈÈˮƿÄÚµÄË®¹¸£ÛÖ÷̉ª³É·ÖMg(OH)2ºÍCaCO3µÈ£Ư£»
¢Ü½đÊôÄÆ×Å»đ¿ÉÓøÉÔïµÄϸɳÆËĂđ£»
¢ƯÔÚËá¼îÖĐºÍµÎ¶¨ÊµÑéÖĐ£¬ÈôµÎ¶¨Ç°×¶ĐÎƿδÓĂ´ư²ẩºÈóÏ´£¬Ộ²â¶¨½á¹ûÆ«Đ¡£»
¢̃½«¸ÉÔïµÄpHÊÔÖ½½₫ÈëijÈÜ̉º̉»»á¶ùºóÈ¡³ö£¬Óë±ê×¼±ÈÉ«¿¨¶ÔƠỞԲⶨ¸ĂÈÜ̉ºpH¡£
¢̣£®Ä³Í¬Ñ§ÎªÑĐ¾¿ÏơËáÓëĂ¾µÄ·´Ó¦£¬½øĐĐͼʾʵÑ飬ʵÑéÏÖÏóÈçÏ£º
(a) AÖĐ×ăÁ¿Ä³Å¨¶ÈµÄÏơËáÓëMgƬ·¢Éú·´Ó¦£¬Éú³ÉµÄÆø̀åͨ¹ưBºó£¬ÔÚBÖĐÖ»Éú³É̉»ÖÖÑΣ¬Ê£ÓàÆø̀åÓö¿ƠÆø²»±äÉ«£»
(b) ´ÓC½øÈëDÖеÄÆø̀åÓĐÁ½ÖÖÇ̉¾ùΪµ¥ÖÊ£»
(c) ½«D¼ÓÈÈ̉»¶Îʱ¼äºó£¬EÖиÉÔïµÄº́ɫʯÈïÊÔÖ½Öđ½¥±äÀ¶¡£
(¼ÙÉèʵÑéÇ°×°ÖĂÖĐµÄ¿ƠÆø̉ÑÅž¡)
̉ÑÖª£º2NO2+2NaOH=NaNO3+NaNO2+H2O£¬NO2+NO+2NaOH=2NaNO2+H2O¡£
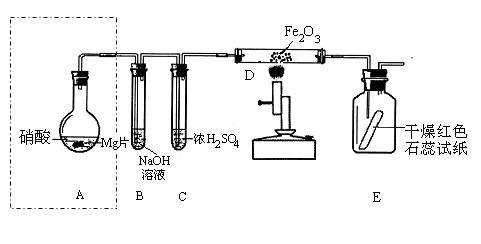
£¨1£©A×°ÖĂËùÉæ¼°µÄʵÑé̉ÇÆ÷Ăû³ÆÓе¼¹Ü¡¢__________________________ ºÍ ______________________¡£
£¨2£©ÏơËáÓëMgƬ·´Ó¦Éú³ÉµÄÆø̀å³É·ÖÊÇ_________________________(ÓĂ»¯Ñ§Ê½±íʾ)¡£
£¨3£©Đ´³öDÖĐ·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽ¢Ù____________________________________£»
¢Ú________________________________________________________________ ¡£
ij»¯Ñ§¿ÎÍâĐ¡×éΪ²â¶¨¿ƠÆøÖĐCO2µÄº¬Á¿£¬½øĐĐÁËÈçÏÂʵÑ飺
¢ÙÅäÖÆ0.1000 mol/LºÍ0.01000 mol/LµÄ±ê×¼ÑÎËᣮ
¢ÚÓĂ0.1000 mol/LµÄ±ê×¼ÑÎËáµÎ¶¨Î´ÖªÅ¨¶ÈµÄBa(OH)2ÈÜ̉º10.00 mL£¬½á¹ûÓĂÈ¥ÑÎËá19.60 mL£®
¢ÛÓĂ²â¶¨µÄBa(OH)2ÈÜ̉ºÎüÊƠ¶¨Á¿¿ƠÆøÖеÄCO2£®È¡Ba(OH)2ÈÜ̉º10.00 mL£¬·ÅÈë100 mLÈƯÁ¿Æ¿Àï¼ÓË®ÖÁ¿̀¶ÈÏߣ¬È¡³öÏ¡ÊͺóµÄÈÜ̉º·ÅÈëĂܱƠÈƯÆ÷ÄÚ£¬²¢Í¨Èë10 L±ê×¼×´¿öϵĿƠÆø£¬Ơñµ´£¬ƠâʱÉú³É³Áµí£®
¢Ü¹ưÂËÉÏÊöËùµĂ×Ç̉º£®
¢ƯÈ¡ÂË̉º20.00 mL£¬ÓĂ0.01000 mol/LµÄÑÎËáµÎ¶¨£¬ÓĂÈ¥ÑÎËá34.80 mL£®Çë»Ø´đÏÂÁĐÎỀ⣺
(1)ÅäÖƱê×¼ÑÎËáʱ£¬ĐèÓĂÏÂÁĐÄÄĐ©̉ÇÆ÷£¿________£»
A£®ÍĐÅ̀̀́ƽ
B£®ÈƯÁ¿Æ¿
C£®ËáʽµÎ¶¨¹Ü
D£®Á¿Í²
E£®ÉƠ±
F£®½ºÍ·µÎ¹Ü
G£®²£Á§°ô
(2)µÎ¶¨²Ù×÷ÖĐ£¬×óÊÖ________£¬Ó̉ÊÖ________£¬ÑÛ¾¦________£»
(3)Ba(OH)2ÈÜ̉ºµÄÎïÖʵÄÁ¿Å¨¶ÈÊÇ________£»
(4)¹ưÂËËùµĂ×Ç̉ºµÄÄ¿µÄÊÇ________£»
(5)´Ë¿ƠÆøÑùÆ·ÖĐº¬CO2µÄ̀å»ư·ÖÊưΪ________£»
(6)±¾ÊµÑéÖĐ£¬ÈôµÚ̉»´ÎµÎ¶¨Ê±Ê¹ÓõÄËáʽµÎ¶¨¹Üδ¾´¦Àí£¬¼´×¢ÈëµÚ¶₫ÖÖ±ê×¼ÑÎËᣬ²¢½øĐеڶ₫´ÎµÎ¶¨£¬Ê¹²â¶¨½á¹û________(̀î¡°Æ«´ó¡±¡°Æ«Đ¡¡±»̣¡°Î̃Ó°Ḯ¡±)£®
̉»£®µ¥ÏîÑ¡Ôñ
1£®D 2£®A 3£®B 4£®B 5£®D 6£®C 7£®B 8£®A
¶₫£®²»¶¨ÏîÑ¡Ôñ
9£®A 10£®BC 11£®AD 12£®AC 13£®CD 14£®B 15£®C 16£®D
Èư£®£¨±¾̀â°üÀ¨2Đ¡̀⣬¹²22·Ö£©
17£®¢Ù¢Û¢Ư¢ß£¨6·Ö£© ˵Ă÷£ºÂ©Ñ¡¡¢´íÑ¡̉»¸ö¾ù¿Û2·Ö£¬¿ÛÍêΪֹ
18£®¢Å·ÖÁ󣨻̣ƠôÁ󣩣¨2·Ö£©
¢Æ¢ÙŨẠ́Ëᣨ1·Ö£© ʹµÎÈëÉƠÆ¿ÖеÄSiHCl3Æø»¯£¨2·Ö£©
¢ÚÓĐ¹̀̀åÎïÖÊÉú³É£¨1·Ö£© ÔÚ1000¡«1100¡æµÄ·´Ó¦Î¶ÈÏ£¬ÆƠͨ²£Á§»áÈí»¯£¨1·Ö£©
SiHCl3£«H2Si£«3HCl£¨3·Ö£©
¢ÛÅž¡×°ÖĂÖĐµÄ¿ƠÆø£¨2·Ö£©
¢Ü½«ÊÔÑùÓĂÏ¡ÑÎËáÈܽ⣬¾²ÖĂÈ¡ÉϲăÇå̉º£¬¼ÓÈëÂÈË®ºóÔٵμӼ¸µÎKSCNÈÜ̉º£¬¹Û²́ÊÇ·ñÓĐº́É«ÈÜ̉ºÉú³É¡££¨4·Ö£©
˵Ă÷£ºÖ»̉ª·½°¸Éè¼Æ¼̣µ¥£¬ÏÖÏóĂ÷ÏÔ£¬ºÏÀí¾ù¿ÉµĂ·Ö¡£
ËÄ£®£¨±¾̀â°üÀ¨2Đ¡̀⣬¹²19·Ö£©
19£®¢ÅµÚÈưÖÜÆÚµÚVIA×壨2·Ö£©
¢ÆC3N4£¨2·Ö£© ´óÓÚ£¨1·Ö£©
¢Ç2Al£«2OH££«2H2O£½2AlO2££«3H2¡ü£¨3·Ö£©
20£®¢ÅNaCl£¨2·Ö£©
¢Æ½µµÍX¡¢YÈÛ»¯Ê±µÄζȣ¬½ÚÔ¼ÄÜÔ´£¨2·Ö£©
¢ÇÓĂ×÷¸ÉÔï¼Á£¨1·Ö£©
¢È2Cl2£«Ca(OH)2£½CaCl2£«Ca(ClO)2£«2H2O£¨3·Ö£©
2Na2O2£«2H2O£½4NaOH£«O2£¨3·Ö£©
Î壮£¨±¾̀â°üÀ¨1Đ¡̀⣬¹²9·Ö£©
21£®¢Å £¼£¨3·Ö£©
¢Æ2C2H6(g)£«7O2(g)£½4CO2(g)£«6H2O(g)£»¦¤H£½£3121.6KJ/mol £¨3·Ö£©
¢ÇÔ½ÉÙ£¨3·Ö£©
Áù¡¢£¨±¾̀â°üÀ¨2Đ¡̀⣬¹²18·Ö£©
22£®¢Å£¨2·Ö£©
¢Æ£¨2·Ö£©
£¨2·Ö£©
¢Ç £¨1·Ö£© £¨1·Ö£©
23£®¢ÅNaOHÈÜ̉º¡¢¡÷£¨2·Ö£© ŨẠ́Ëá ¡¢¡÷£¨2·Ö£©
¢ÆA£º £¨2·Ö£© F£º £¨2·Ö£©
¢Ç2£«O22 £«2H2O£¨2·Ö£©
Æß¡¢£¨±¾̀â°üÀ¨2Đ¡̀⣬¹²18·Ö£©
24£®¢Å1:1£¨2·Ö£©
¢Æ0.71£¨3·Ö£©
¢Ç6g£¨3·Ö£©
25£®¢Å2.75mol/L£¨3·Ö£©
¢Æ0£¨3·Ö£©
½âÎö£ºÉè12.8gµÄÑùÆ·ÖĐCuSµÄÎïÖʵÄÁ¿Îªx £¬Cu2SµÄÎïÖʵÄÁ¿Îªy
96x£«160y£½12.8
8x/3£«10y/3£½0.3
½âµĂ£ºx£½y£½0.05mol
¸ù¾Ư·½³̀ʽ¢Ù¡¢¢Ú¿ÉÖªÏûºÄn(H£«)£½0.05mol¡Á8/3£«0.05mol¡Á16/3£½0.4mol
¹ÊÊ£Óàn(H£«)£½0.1mol£¬c(H£«)£½1mol/L pH£½0
¢Ç11.2L£¨4·Ö£©
½âÎö£ºÊ×ÏÈÅжÏ64gÑùÆ·ÖĐCuS¡¢Cu2SµÄÎïÖʵÄÁ¿Îª0.25mol
±¾̀â²ÉÓĂ¼«¶Ë¼ÙÉ裺
ÈôHNO3¾ùÓëCuS·´Ó¦£ºÏơËá²»×ă£¬ỘV(NO)£½0.5mol¡Á22.4L/mol£½11.2L
ÈôHNO3¾ùÓëCu2S·´Ó¦£ºÏơËá²»×ă£¬ỘV(NO)£½0.5mol¡Á22.4L/mol£½11.2L
Ëù̉Ô£ºcÖĐ²úÉúÆø̀å̀å»ư£¨V£©µÈÓÚ11.2L¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com