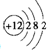
A、B、C三种常见物质中均含有同一种元素,它们之间有如图1所示的转化关系(部分反应物质已略去).
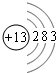
(1)若A是一种两性氧化物,B的水溶液呈酸性,C的水溶液呈碱性,请写出A、B、C三种物质中含有的同一种金属元素的原子结构示意图
B溶液显酸性的原因(用离子方程式表示)
Al3++3H2O?Al(OH)3+3OH-
Al3++3H2O?Al(OH)3+3OH-
,反应④的离子方程式
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.
(2)若A为一种金属单质时,反应①②③均为化合反应,反应④为置换反应.请写出③可能的离子方程式
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
和工业冶炼A的化学方程式
.
(3)若A、B、C是三种不同类别的固态物质,C是一种既含有离子键又含有共价键的化合物,溶于水电离出两种相同电子数的离子,B是工业上制取A、C的原料.实验室保存少量单质A的方法是
通常将Na保存保存在煤油或石蜡油当中
通常将Na保存保存在煤油或石蜡油当中
.写出工业采用B制取C的离子方程式
;
(4)若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液pH<7,将C通入A溶液中,pH值先增大后减小.
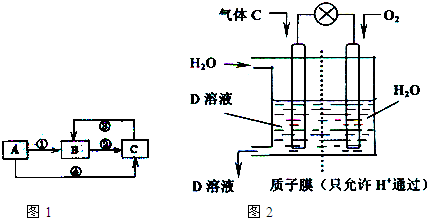
①将C通入如图2所示装置中,可以制得强电解质D的溶液,写出气体C发生的电极反应式
2SO2-4e-+4H2O=2SO42-+8H+
2SO2-4e-+4H2O=2SO42-+8H+
②该装置中H
+的作用是
使电解质溶液导电
使电解质溶液导电
③若转移的电子数为6.02×10
22时,左槽n(H
+)的变化量为
0.2mol
0.2mol
.

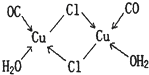


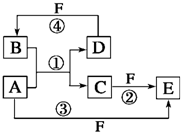 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).