
题目列表(包括答案和解析)
(10分)处于相邻两个周期的主族元素A、B、C、D,它们的原子半径依次变小;A离子和B离子的电子层相差两层,且能形成BA2型的离子化合物;C的离子带3个正电荷且核外电子排布与氖相同;D气态氢化物的分子式为H2D,D在它的最高价氧化物中的质量分数是40%且D原子核中有16个中子。试回答:
(1)按要求填空:
A元素的名称 B元素的符号
C原子的外围电子排布式为 D的原子结构示意图
(2)B、C、D的第一电离能由大到小的顺序是: (填元素符号)
(3)A、B、C的电负性由大到小的顺序是: (填元素符号)
(4)A与B形成的化合物的电子式
(5)将C投入到的KOH溶液中现象为 ,相应的离子反应方程式为 。(2分)
处于相邻两个周期的主族元素A、B、C、D,它们的原子半径依次变小.A离子和B离子相差两个电子层,且能形成 型离子化合物.C的离子带3个正电荷.D的气态氢化物通式为
型离子化合物.C的离子带3个正电荷.D的气态氢化物通式为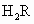 ,在最高价氧化物中,D含量为40%,D的原子序数大致等于其相对原子质量数值的一半.试回答(写名称、符号):
,在最高价氧化物中,D含量为40%,D的原子序数大致等于其相对原子质量数值的一半.试回答(写名称、符号):
(1)A是________元素,在周期表的位置________;
B是________元素,在周期表的位置________;
C是________元素,在周期表的位置________;
D是________元素,在周期表的位置________.
(2)B、C、D单质的还原性从大到小的顺序是________.
| A.Y、Z的氧化物都有两性 |
| B.气态氢化物的稳定性:Z>X |
| C.原子半径:W>Y>Z>X |
| D.最高价氧化物对应水化物的碱性:W<Y |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com