
题目列表(包括答案和解析)
(15 分)
A、B、C、D均是前四周期元素组成的单质或化合物。它们之间有如下转化关系:
![]()
(1) 若A是某矿石的主要成份,上述转化关系表示工业生产D的过程,且反应②在接触室中进行,反应①在______(填设备名称)中进行。工业上使用______吸收C,以提高吸收效率。
(2) 若D是能使澄清石灰水变浑浊的无色无味气体,A、B为两种单质,组成它们的元素原子序数之和为18,②、③均为化合反应,则反应①中氧化剂与还原剂的质量之比为______
(3) 若A、B、C、D均含有同一种常见金属元素,B是黑色磁性固体,D是一种红褐色沉淀,反应②在常见稀酸中进行,C是该反应中生成的唯一盐,反应②的离子方程式是______检验C中金属阳离子的常见试剂是______(填名称)。
(4) 若A、B、C、D均含有同一种短周期的金属元素,且B和D在溶液中反应生成沉淀C,则下列判断正确的是______ (填字母)。
a. A可能是一种耐火材料;
b. B的溶液一定呈碱性;
c. C 一定既溶于盐酸又溶于苛性钠溶液;
则B与D在溶液中反应的离子方程式为________________________。
现有A、B、C、D、E五种物质,它们有如下反应关系:
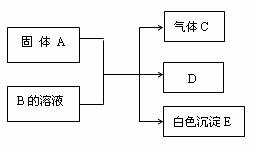
(1)若A是由短周期中原子半径最大的元素与地壳中含量最多的元素组成的离子化合物,且两种元素的原子个数比为1:1。则A中存在的化学键是 、 。
(2)若A是可溶性强碱,B是正盐,E不溶于稀硝酸,则B的化学式为 ,
(3)若A是NaHCO3,B是正盐,E既可溶于盐酸又可溶于NaOH溶液,该反应的离子方程式为 。
(4)若C是一种四原子分子,燃烧时有浓烈的黑烟。A与B的溶液反应时只生成气体C、CaCO3和H2O。
①C的电子式为 ;
B的名称为 。
②若在标准状况下,用下图的装置进行实验,欲测定某电石试样中 A 的质量分数,请回答下列问题:
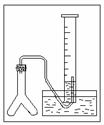
若反应刚结束时,观察到的实验现象如图所示,这时不能立即读数,应待 以后再进行的操作是: ,之后读出气体的体积是d L,如果电石试样质量为 c g,则电石试样中 A 的质量分数的计算式W ( A )= (杂质所生成的气体体积忽略不计)。
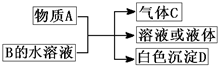
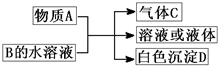 (2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
(2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
| ||
| ||
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
| 浓硝酸 |
| 一定量NaOH |
| D的溶液 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com