A、B、C、D、E是五种常见的短周期主族元素,它们的原子序数依次增大,其中A与C、B与D分别同族,已知B、D两种元素原子核中质子数之和是A、C两种元素原子核中质子数的2倍,五种元素中只有一种为金属元素.请回答下列问题
(1)物质甲、乙是由上述五种元素中的两种元素形成的常温下为液体的化合物,则甲、乙的化学式
H2O或H2O2
H2O或H2O2
、
H2O2或H2O
H2O2或H2O
,写出其中一种物质使酸性KMnO
4溶液褪色的离子反应方程式
5H2O2+2MnO4-+6H+═2Mn2++8H2O+5O2↑
5H2O2+2MnO4-+6H+═2Mn2++8H2O+5O2↑
.
(2)已知:2DB
2+B
2
2DB
3,若3.2gDB
2完全转化为DB
3气体时放热akJ;1mol DB
3气体完全转化为其水化物放热bkJ,则标况下33.6L DB
2完全完成上述两步反应放热
(30a+1.5b)
(30a+1.5b)
kJ(用a、b表示),我国工业生成DB
2所用的原料是
FeS2
FeS2
(填化学式)
(3)丙、丁两化合物均由A、B、C、D四种元素组成,写出丙丁两化合物反应的化学反应方程式:
NaHSO4+NaHSO3═Na2SO4+SO2↑+H2O
NaHSO4+NaHSO3═Na2SO4+SO2↑+H2O
.
(4)将一定量的DB
2通入到紫色石蕊试液中的现象是:
溶液变为红色
溶液变为红色
.再通入等物质的量E
2所观察的现象是
溶液仍为红色
溶液仍为红色
.
(5)用A、B两元素的单质可制成新型化学电源,若以C的最高价氧化物的水化物为电解质,则通A的一极的电极反应方程式:
H2+2OH--2e-→2H2O
H2+2OH--2e-→2H2O
.若以此电源进行铁片上镀铜,若两极质量差为6.4g时,理论上消耗标况下
1.12
1.12
L的A单质.

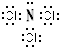
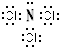


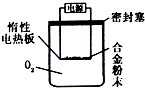 短周期主族元素A、B、C、D的原子序数依次增大,它们的原子核外电子层数之和为7.B的化合物种类繁多,数目庞大.A与D能形成原子个数比为1:l和2:l的化合物.
短周期主族元素A、B、C、D的原子序数依次增大,它们的原子核外电子层数之和为7.B的化合物种类繁多,数目庞大.A与D能形成原子个数比为1:l和2:l的化合物. 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热