АБгазХЙуЗКЕФгУЭОЃЌШчПЩгУгкЛЏЗЪЁЂЯѕЫсЁЂКЯГЩЯЫЮЌЕШЙЄвЕЩњВњЃЎАБЕФЫЎШмвКжаДцдкЕчРыЦНКтЃЌГЃгУЕчРыГЃЪ§K
bКЭЕчРыЖШІСРДЖЈСПБэЪОЦфЕчРыГЬЖШЃЎK
bКЭІСГЃгУЕФВтЖЈЗНЗЈЃКдквЛЖЈЮТЖШЪБгУЫсЖШМЦВтЖЈвЛЯЕСавбжЊХЈЖШАБЫЎЕФpHЃЌПЩЕУИїХЈЖШАБЫЎЖдгІЕФcЃЈOH
-ЃЉЃЌШЛКѓЭЈЙ§ЛЛЫуЧѓЕУИїЖдгІЕФІСжЕКЭK
bжЕЃЎ
ЯТУцЪЧФГжабЇЛЏбЇаЫШЄаЁзщдк25ЁцЪБВтЖЈвЛЯЕСаХЈЖШАБЫЎЕФpHЫљЖдгІЕФcЃЈOH
-ЃЉЃК
[вЧЦїгыЪдМС]ЫсЖШМЦЁЂ50mLМюЪНЕЮЖЈЙмЁЂ100mLЩеБЁЂ0.10mol?L
-1 АБЫЎ
[ЪЕбщЪ§Он]ЃЈВЛБиЬюБэИёЃЉ
| ЩеБКХ |
VАБЫЎ ЃЈmLЃЉ |
VЫЎЃЈmLЃЉ |
c ЃЈNH3?H2OЃЉ ЃЈmol?L-1ЃЉ |
cЃЈOH-ЃЉ |
Kb |
ІС |
| 1 |
50.00 |
0.00 |
|
1.34ЁС10-3 |
|
|
| 2 |
25.00 |
25.00 |
|
9.48ЁС10-4 |
|
|
| 3 |
5.00 |
45.00 |
|
4.24ЁС10-4 |
|
|
ЧыИљОнвдЩЯаХЯЂЛиД№ЯТЪіЮЪЬтЃК
ЃЈ1ЃЉ25ЁцЪБЃЌАБЫЎЕФЕчРыГЃЪ§ЃКK
bЁж______ЃЌЭЈЙ§МЦЫуЫљЕУЕФЪ§ОнКЭМђНрЕФЮФзжЫЕУїЕчРыГЃЪ§ЁЂЕчРыЖШгыШѕЕчНтжЪЕФГѕЪМХЈЖШЕФЙиЯЕ______
ЃЈ2ЃЉгУ0.10mol?L
-1бЮЫсЗжБ№ЕЮЖЈ20.00mL0.10mol?L
-1ЕФNaOHШмвККЭ20.00mL0.10mol?L
-1АБЫЎЫљЕУЕФЕЮЖЈЧњЯпШчЯТЃК
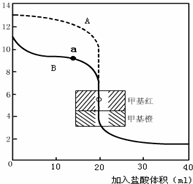
ЧыжИГібЮЫсЕЮЖЈАБЫЎЕФЧњЯпЮЊ______ЃЈЬюAЛђBЃЉЃЌЧыаДГіЧњЯпaЕуЫљЖдгІЕФШмвКжаИїРызгХЈЖШгЩДѓЕНаЁЕФХХСаЫГађ______ЃЎ
ЃЈ3ЃЉвКАБзїЮЊвЛжжЧБдкЕФЧхНрЦћГЕШМСЯвбдНРДдНБЛбаОПШЫдБжиЪгЃЎЫќдкАВШЋадЁЂМлИёЕШЗНУцНЯЛЏЪЏШМСЯКЭЧтШМСЯгазХНЯДѓЕФгХЪЦЃЎАБдкШМЩеЪдбщЛњжаЯрЙиЕФЗДгІгаЃК
4NH
3ЃЈgЃЉ+3O
2ЃЈgЃЉ=2N
2ЃЈgЃЉ+6H
2OЃЈlЃЉЁїH
1Ђй
4NH
3ЃЈgЃЉ+5O
2ЃЈgЃЉ=4NOЃЈgЃЉ+6H
2OЃЈlЃЉЁїH
2Ђк
4NH
3ЃЈgЃЉ+6NOЃЈgЃЉ=5N
2ЃЈgЃЉ+6H
2OЃЈlЃЉЁїH
3Ђл
ЧыаДГіЩЯЪіШ§ИіЗДгІжаЁїH
1ЁЂЁїH
2ЁЂЁїH
3Ш§епжЎМфЙиЯЕЕФБэДяЪНЃЌЁїH
1=______ЃЎ
ЃЈ4ЃЉAllis-ChalmersжЦдьЙЋЫОЗЂЯжПЩвдгУАБзїЮЊШМСЯЕчГиЕФШМСЯЃЎЦфзмЗДгІЪНЮЊ4NH
3+3O
2=2N
2+6H
2OЃЌе§МЋЩЯЕФЕчМЋЗДгІЪНЮЊO
2+
2H
2O+4e
-=4OH
-ЃЌдђИКМЋЩЯЕФЕчМЋЗДгІЪНЮЊ______ЃЎ

