
题目列表(包括答案和解析)
| 实验操作 | 预期现象和结论 |
| 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤. | 粉末减少,说明粉末可能含有Al2O3 |
| 步骤2:取少量步骤1的滤液于试管中,逐滴滴加3mol/L盐酸至过量. | 有白色沉淀产生然后沉淀又溶解 有白色沉淀产生然后沉淀又溶解 ,说明粉末中含有Al2O3. |
| 步骤3:将步骤1的滤渣转移到烧杯B中,加入足量3mol/L CuSO4,充分搅拌,过滤,洗涤. | 有红色固体生成,说明粉末中含有 Fe Fe . |
| 步骤4: 将步骤3的滤渣转移到烧杯C中, 加入足量3mol/L盐酸,静置,取上层清液, 滴加适量的双氧水,充分振荡后滴加KSCN 溶液. 将步骤3的滤渣转移到烧杯C中, 加入足量3mol/L盐酸,静置,取上层清液, 滴加适量的双氧水,充分振荡后滴加KSCN 溶液. |
固体部分溶解,溶液变血红色,说明粉 末中含有FeO 固体部分溶解,溶液变血红色,说明粉 末中含有FeO |
(15分)某化学研究小组探究无水三草酸合铁酸钾K3[Fe(C2O4)3]受热分解的产物,并对所得气体产物和固体产物进行验证,按下图装置进行实验(夹持仪器已略去)。
(1)连接好装置后,加入药品前,应该进行的实验操作是________________(填操作名称)。
(2)实验开始时缓缓通入氮气,过一段时间以后,加热反应管A和E ,待反应完全后,停止加热,仍继续通氮气,直到反应管冷却。停止加热前是否需要先断开A、B的连接处和E、F的连接处?为什么?_______________________________________________________________。
(3)实验中观察到B中澄清石灰水变浑浊,则说明气体产物中有 (写化学式)。
能证明分解产物中有CO气体生成的实验现象是 。
(4)该小组同学查阅资料后得知,固体产物中不存在+3价Fe元素,而盐类物质只有K2CO3。
① 验证固体产物中钾元素存在的方法是 ,现象是 。
② 研究小组为探究铁元素的存在形式,取A中充分反应后所得固体于试管中,加入足量蒸馏水,过滤、洗涤、干燥得到黑色粉末,取4.4g黑色粉末溶于足量稀硝酸中,收集到标准状况下NO气体1.12L通过计算判断黑色粉末的成分为 (写化学式)。写出黑色粉末溶于足量稀硝酸发生反应的离子方程式 。
(15分)某化学研究小组探究无水三草酸合铁酸钾K3[Fe(C2O4)3]受热分解的产物,并对所得气体产物和固体产物进行验证,按下图装置进行实验(夹持仪器已略去)。

(1)连接好装置后,加入药品前,应该进行的实验操作是________________(填操作名称)。
(2)实验开始时缓缓通入氮气,过一段时间以后,加热反应管A和E ,待反应完全后,停止加热,仍继续通氮气,直到反应管冷却。停止加热前是否需要先断开A、B的连接处和E、F的连接处?为什么?_______________________________________________________________。
(3)实验中观察到B中澄清石灰水变浑浊,则说明气体产物中有 (写化学式)。
能证明分解产物中有CO气体生成的实验现象是 。
(4)该小组同学查阅资料后得知,固体产物中不存在+3价Fe元素,而盐类物质只有K2CO3。
① 验证固体产物中钾元素存在的方法是 ,现象是 。
② 研究小组为探究铁元素的存在形式,取A中充分反应后所得固体于试管中,加入足量蒸馏水,过滤、洗涤、干燥得到黑色粉末,取4.4g黑色粉末溶于足量稀硝酸中,收集到标准状况下NO气体1.12L通过计算判断黑色粉末的成分为 (写化学式)。写出黑色粉末溶于足量稀硝酸发生反应的离子方程式 。
(13分)某化学兴趣小组的同学用下图所示实验装置进行实验研究(图中a、b、c表示止水夹),请对其方案进行完善或评价。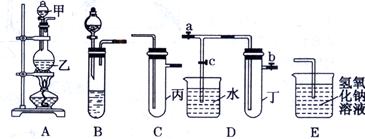
(1)实验室将B、C、E相连后,以浓盐酸和 为原料可制取Cl2。
(2)利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作如下,将现象①填入下表:
| 实验 序号 | 实验操作 | 现象 |
| Ⅰ | 将氯水滴入品红溶液 | ① |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com