已知:短周期元素A、B、C、D、E原子序数依次增大.
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
(1)B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是______(用离子方程式表示).
(2)常温下,若甲、丙两溶液的pH均等于5,则由水电离出的c(H
+)
甲:c(H
+)
丙=______;
(3)盐丙中含有的化学键是______.
(4)0.1mol D单质和0.2mol E单质组成的混合物投入到足量的A
2C中,产生气体的体积(标准状况)是______.
(5)反应:乙+C
2→B
2+A
2C(未配平)可设计为燃料电池,则通入乙的电极是______极(填“正”或“负”),在碱性条件下其电极反应是______.
(6)已知
xC和
yC是C元素的两种核素,N
A表示阿伏加德罗常数,下列说法正确的是______.
A.
xC
2与
yC
2互为同分异构体
B.
xC与
yC核外电子排布方式不同
C.通过化学变化可以实现
xC与
yC间的相互转化
D.标准状况下,1.12L
xC
2和1.12L
yC
2均含有0.1N
A个C原子.

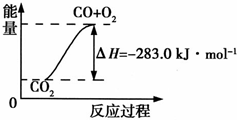 已知:①CO(g)+
已知:①CO(g)+


 NaClO3 + 3H2↑
NaClO3 + 3H2↑