
题目列表(包括答案和解析)
某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下:
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 65 | 249 | 199.6 |
Ⅰ、合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.4g苯甲酸和20ml甲醇(密度约为0.79/cm3),再小心加入3ml浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)简述液体混合时,最后加入浓硫酸的理由是 。
(2)若反应产物水分子中有18O,写出能表示瓜在前后18O位置的化学方程式:
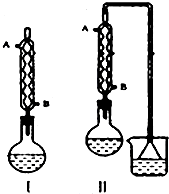
(3)甲、乙、丙三位同学分别设计了如图三套实验室制取苯甲酸和甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的特点,最好采用 装置(填“甲”、“乙”、“丙”)。
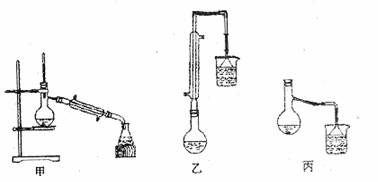
(4)计算可知,反应物甲醇过量,而反应物甲醇应过量,其理由是 。
Ⅱ、粗产品的精制
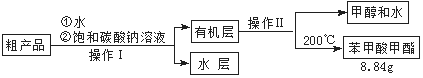
(5)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现似用下列流程图进入精制,请根据流程图填入恰当操作方法的名称:操作1为 ,操作2为
。
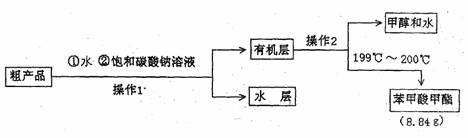
(6)通过计算,苯甲酸甲酯的产率为 。
某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20ml甲醇(密度约0.79g·mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。‘
(1)浓硫酸的作用是 ;
 简述混合液体时最后加入浓硫酸的理由: 。
简述混合液体时最后加入浓硫酸的理由: 。
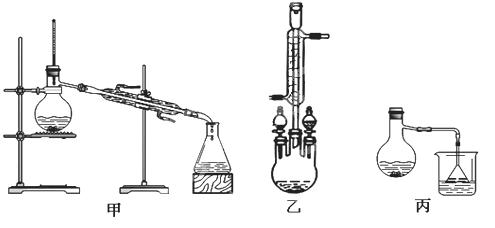
(2)甲、乙、丙三位同学分别设计了如下图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用 装置(填“甲”或“乙”或“丙”)。

Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称。操作Ⅰ 操作Ⅱ 。
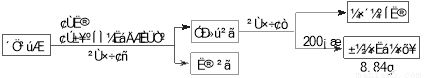
(4)能否用NaOH溶液代替饱和碳酸钠溶液? (填“能”或“否”),
并简述原因 。
(5)通过计算,苯甲酸甲酯的产率是 。
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
|


某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
|
 由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:
由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:| 浓H2SO4 |
| △ |
| ||
| △ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com