
题目列表(包括答案和解析)
I.恒温、恒压下,在一个可变容积K*s^5#u的容器中发生如下发应:A(气)+B(气)![]() C(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时AK*s^5#u的物质K*s^5#u的量
为 mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成CK*s^5#u的物质K*s^5#u的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和CK*s^5#u的物质K*s^5#u的量分别是ymol和3a mol,则x= mol,y= mol。平衡时,BK*s^5#u的物质K*s^5#u的量
(甲) >2 mol (乙)=2 mol (丙)< 2 mol (丁)可能大于、等于或小于2mol
(4)若在(3)K*s^5#u的平衡混合物中再加入3molC,待再次到达平衡后,CK*s^5#u的物质K*s^5#u的量分数是 。
(5)若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定K*s^5#u的容器中发生上述反应。开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中K*s^5#u的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和bK*s^5#u的大小
(6) A(气)+B(气)![]() C(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新K*s^5#u的平衡时,BK*s^5#u的浓度是原来K*s^5#u的60%,则
C(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新K*s^5#u的平衡时,BK*s^5#u的浓度是原来K*s^5#u的60%,则
A.平衡向正反应方向移动了 B.物质AK*s^5#u的转化率增大了
C.物质BK*s^5#u的质量分数增加了 ![]() 混合气体K*s^5#u的平均相对分子质量减少了
混合气体K*s^5#u的平均相对分子质量减少了
II. 某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
一级电离:H2A![]() H++HA- 二级电离:HA-
H++HA- 二级电离:HA-![]() H++A2-
H++A2-
已知相同浓度时K*s^5#u的电离度a(H2A)>d(HA-),设有下列四种溶液:
A.0.01mol.L-1K*s^5#u的H2A溶液 B.0.01mol.L-1K*s^5#u的NaHA溶液
C.0.01mol.L-1K*s^5#u的HCl与0.04mol.L-1K*s^5#u的NaHA溶液等体积混合液
D.0.02mol.L-1K*s^5#u的NaOH与0.02 mol.L-1K*s^5#u的NaHA溶液等体积混合液
![]()
![]() 据此,填写下列空白(填代号)
据此,填写下列空白(填代号)
(1) c(H+)最大K*s^5#u的是__________,最小K*s^5#u的是__________。
(2) c(H2A)最大K*s^5#u的是_________,最小K*s^5#u的是__________
(3) c(A2-)最大K*s^5#u的是___________, 最小K*s^5#u的是________。
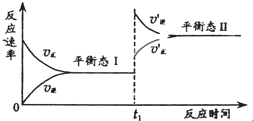 如图所示,一定条件下,某密闭容器中的可逆反应R(s)+X(g)﹦Y(g)+Z(g);△H>0达到平衡态I后,在t1时刻改变影响平衡的一个条件,平衡发生移动,达到平衡态II.则t1时刻的条件改变可能是( )
如图所示,一定条件下,某密闭容器中的可逆反应R(s)+X(g)﹦Y(g)+Z(g);△H>0达到平衡态I后,在t1时刻改变影响平衡的一个条件,平衡发生移动,达到平衡态II.则t1时刻的条件改变可能是( )| A、升高温度 | B、减小体积 | C、增大Y的浓度 | D、加入一定量的R |
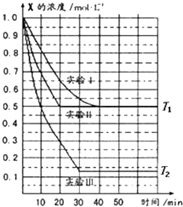 (2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( )
(2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( ) 2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线
2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线
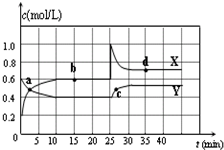 I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中, 2X
2X 2X
2X 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是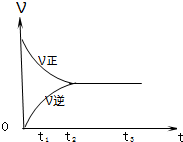
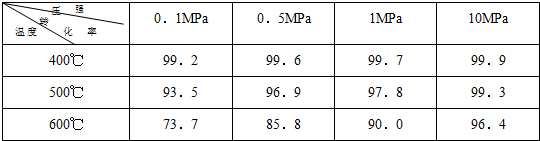
 2SO3 的两个素材:
2SO3 的两个素材: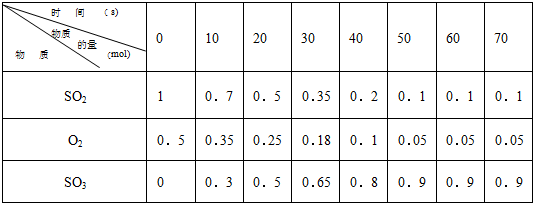
15、(12分) (1)Mg2+、Al3+、NO 、SO
、SO (4分)
(4分)
(2)Fe2+、Ba2+、I-、HCO (4分)
(4分)
(3)焰色反应,取少量原溶液,加入Ba(NO3)2溶液后,取上层清液加入AgNO3溶液和稀HNO3(4分)
16、⑴C、D、F、E; ⑵10;⑶浓硫酸,干燥SO2 ⑷A、D ⑸⑤
⑹42%(或0.42);NaCl、Na2SO4
17、I.(1)溶液显色所需要的时间。
(2)①2NO+O2+4CO 4CO2+N2(3分);②-1160 kJ?mol-1;
4CO2+N2(3分);②-1160 kJ?mol-1;
(3)①该研究只能提高化学反应速率,不能使化学平衡发生移动、 D
II.NO2(2)NH4NO3 N2O+2H2O(3分)
N2O+2H2O(3分)
18、 (1) 、
、 、Mg2+(2)氟,2H2O+
、Mg2+(2)氟,2H2O+
(3)  2CO↑+Si (4)2Mg+CO2
2CO↑+Si (4)2Mg+CO2 2MgO+C
2MgO+C
19、Ⅰ.
 Ⅱ.(1)HgCl2 HgCl++Cl―(1分);
Ⅱ.(1)HgCl2 HgCl++Cl―(1分);
2Fe2++2HgCl2=Hg2Cl2↓+2Fe3++2Cl―(2分);
K=[Fe3+]2―[Cl―]2/[Fe2+]2[HgCl2]2(2分)
(2)不能。因为加热能促进氯化铝水解,且氯化氢逸出也使平衡
|