
题目列表(包括答案和解析)

氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
请回答下列问题:
⑴写出铬原子的基态电子排布式_____________________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有__________(填元素符号),其中一种金属的晶胞结构如右图所示,该晶胞中含有金属原子的数目为 。
⑵CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是__________(填“极性”或“非极性”)分子。
⑶在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。

 氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
氧化剂或氯化剂,能与许多有机物反应。请回答下列问题: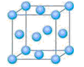
 分子的空间构型是_______。
分子的空间构型是_______。 成的合金。
成的合金。 态碳(C)原子的价电子排布式为 。
态碳(C)原子的价电子排布式为 。 )4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。
)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。 种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中
种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中 每个镁原子周围距离最近的镍原子有 个。
每个镁原子周围距离最近的镍原子有 个。
过渡元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出B元素在周期表中的位置为 ,A2+在基态时外围电子(价电子)排布式为 。
(2)氯化铬酰(CrO2Cl2)熔点:-96 .5℃,沸点:117℃,能与CH3COCH3(丙酮)、CS2等互溶。则固态CrO2Cl2属于 晶体。已知CS2与NO2+互为等电子体,则1mol NO2+中含有π键数目为 。
(3)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
a.水的沸点比甲醛高得多,是因为水分子间能形成氢键
b.甲醛、苯和二氧化碳中碳原子均采用sp2杂化
c.苯、二氧化碳是非极性分子,水和甲醛是极性分子
(4)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。请写出该盐溶解于水后的电离方程式: 。
过渡元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出B元素在周期表中的位置为 ,A2+在基态时外围电子(价电子)排布式为 。
(2)氯化铬酰(CrO2Cl2)熔点:-96 .5℃,沸点:117℃,能与CH3COCH3(丙酮)、CS2等互溶。则固态CrO2Cl2属于 晶体。已知CS2与NO2+互为等电子体,则1mol NO2+中含有π键数目为 。
(3)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
a.水的沸点比甲醛高得多,是因为水分子间能形成氢键
b.甲醛、苯和二氧化碳中碳原子均采用sp2杂化
c.苯、二氧化碳是非极性分子,水和甲醛是极性分子
(4)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。请写出该盐溶解于水后的电离方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com