
题目列表(包括答案和解析)
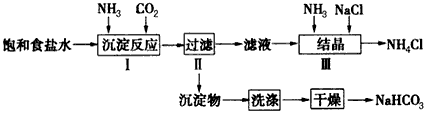

试简述将浓氨水滴入锥形瓶中的操作:_________________。
(2)若用图2装置进行该沉淀反应,反应方程式为:NaCl +NH3+CO2+H2O=NaHCO3↓+NH4Cl。实验时,须先从______(填“a”、“b”或“c”)口通入__________。
(3)步骤Ⅲ向滤液中通入氨气,加入细小食盐颗粒,可使NH4Cl晶体单独结晶析出。
①已知四种相关物质不同温度下的溶解度曲线如图3所示,则结晶时宜采用________(填“蒸发结晶” 或“降温结晶”)。
②某同学设计了如图4所示的装置来验证所得的晶体中含有NH4+。
具体操作:取少量晶体于硬质试管中,对晶体部位加热。并在____(填“A”或“B”)处放置____ 试纸,观察现象。
(4)请按提示完成NaHCO3含量分析的实验设计。
试剂:盐酸、澄清石灰水、氢氧化钡溶液、蒸馏水;仪器:电子天平、烧杯、漏斗、玻璃棒、干燥器等。
①准确称量ag样品溶于水,加入足量沉淀剂。沉淀剂最好选用____。
A.Ca(OH)2溶液 B.CaCl2溶液 C.BaCl2溶液 D.Ba(OH)2溶液
②过滤、洗涤、烘干,冷却、称量,称得固体质量为bg。
③重复以上“烘干,冷却、称量”操作,直至____ 为止。此时称得固体质量为cg。
④计算:样品中NaHCO3的含量为____。
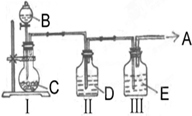 (1)实验室中制取少量干燥纯净的气体A,可用如图装置.
(1)实验室中制取少量干燥纯净的气体A,可用如图装置.(1)实验室中制取少量干燥纯净的气体A,可用如图装置
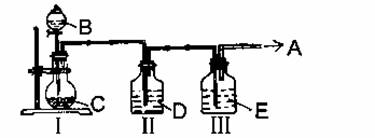
说明:Ⅰ中的漏斗为分液漏斗,转动活塞可以控制液体滴加的速率
①若A可以灭火,则A物质是 ,D物质是 ,II的作用是 ,E物质是 ,Ⅰ中反应的离子方程式为 。
②若C物质是淡黄色粉末,则不需要Ⅲ装置,A物质是 ,B物质是 。
Ⅰ中反应的离子方程式为 。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解 C.蒸发结晶法 D.分液法 E.渗析法 F.蒸馏法 G.过滤法
① ___________从氯化钠溶液中获得氯化钠固体;
② ___________分离溴水中的溴和水;
③ ___________分离水和酒精;
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
12.5 12.5 |
250 250 |
烧杯、玻璃棒、胶头滴管 烧杯、玻璃棒、胶头滴管 |

一、
题号
1
2
3
4
5
答案
A
D
C
B
C
二、
题号
6
7
8
9
10
11
12
13
14
15
16
17
答案
D
D
C
C
D
B
D
B
B
D
C
D
三、
题号
18
19
20
21
22
答案
C
AD
AC
C
BD
四、(本题共24分)
23、(每空1分,共8分)
(1)N , S
⑵ SiO2,SiO2是原子晶体,而CO2是分子晶体; H2O,水分子间作用力大于H2S分子间作用力; (3) Na2O2 (或FeS2;Na2SX等等,填写任意一个正确的即可);
(4) 
 24、(本题共8分)
24、(本题共8分)
(1) (方程式 1分,配平 1分,电子转移方向与数目 2分)
(2) SnCl2 , 3×6.02×1023 (每空1分,共2分) (3)1:1 (2分)
25、(本题共8分)
(1)放热 (1分)  (2)① 0.0175mol/L•min (1分) ②平衡(1分)
(2)① 0.0175mol/L•min (1分) ②平衡(1分)
③ 是 ,等于 ,
(每空1分,共3分) ④ a、b (2分)
五、(本题共24分)
26、(本题共12分)
(1)吸收空气中的CO2, 偏高 (每空1分,共2分)
(2)装置C反应前后质量 (1分)
(3),(5×c×v×10-3×84 )/ m1 (2分)
(4)NaHCO3(其他合理答案也可)(1分)(5)b (1分) (6)蒸发 (1分)
(7)烧杯、酒精灯 (每空1分,共2分) (8)偏高 (2分)
27、(本题共12分)
(1) 把装置中的空气赶走,防止NO被氧化为NO2 ,干燥反应中生成的气体 (每空1分,共2分) (2) 无色气体变为红棕色 ,热 (每空1分,共2分)
(3) 打开K1、K2持续通入一段时间的N2和O2 (2分)
(4)① 0.5 ②C中烧瓶在实验前后增加的质量 (每空2分,共4分)
(5)在A中加入过量含Cl-溶液,过滤后,将沉淀洗涤、干燥,最后称取沉淀的质量(2分)
(其他合理答案也可)
六、(本题共20分)
 28、(本题共8分)
28、(本题共8分)
(1)(各1分,共2分)
(2)(各1分,共2分)消去反应 酯化反应(或取代反应)
(3)(各2分,共4分)


29.(本题共12分)
(1)羟基 羧基
(各1分,共2分) (2分)
(2分)
 (2)HOCH2―CH2OH+O2
OHC―CHO+2H20 (2分) (3)B E (2分)
(2)HOCH2―CH2OH+O2
OHC―CHO+2H20 (2分) (3)B E (2分)
(4)(各2分,共4分) 
 (其他合理答案也可)
(其他合理答案也可)
七、(本题共16分)
30、(本题共6分)
(1)x=1 (2分)
(2)14.4 (2分)
(3)6 (2分)
31、(每空2分,共10分)
(1).2.8×105 ;18
(2).86.96%
(3). ;138
;138
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com