
题目列表(包括答案和解析)
(海南省万宁市2008届高三年级第一学期期中考试,化学,17)(1)中和热的测定实验(如图)。
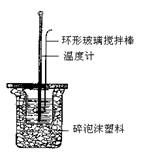
①量取反应物时,取50mL0.50mol·L-1的盐酸,还应加入的试剂是 (填序号)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
②在实验过程中,该同学需要测定并记录的实验数据有 (填序号)。
A.盐酸的浓度 B.盐酸的温度
C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度
E.水的比热容 F.反应后混合溶液的终止温度
③若用50mL0.5mol·L-1醋酸溶液代替上述盐酸测定中和热,所得数据 。(填“偏大”或“偏小”或“不变”)
(2)硫酸铜晶体(CuSO4·xH2O)结晶水含量的测定实验。
①称量一定质量硫酸铅晶体后,加热脱结晶水时用到的仪器主要有:玻璃棒、三角架、坩埚、坩埚钳、泥三角和 。
②实验中要将坩埚放在干燥器中冷却,其主要目的是
。
③若坩埚的质量为m,坩埚与硫酸铜晶体的质量为m1,加热后坩埚与无水硫酸铜的质量为m2,则晶体CuSO4·xH2O中x= (写表达式)。
④如果实验中加热温度过高,固体颜色变黑,则测定结果会 (填“不变”或“偏高”或“偏低”)。
(宁夏银川市实验中学2009届高三年级第三次月考,化学,5)离子检验的常用方法有三种:
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法不合理的是
A.NH4+-气体法 B.I--沉淀法
C.Fe3+-显色法 D.Ca2+-气体法
(浙江春晖中学高三年级2008学年第一学期十二月月考,化学,8)下列实验操作正确的是
①氯水存放于棕色广口瓶中 ②可用氯化铁溶液除去试管内难以刷去的铜迹 ③在200 mL 烧杯中,加入80 mL 水和20g KNO3晶体,配制质量分数约为20%的KNO3溶液。 ④取钠切割后,将剩余的钠块放入废液缸 ⑤分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 ⑥在500 mL容量瓶中加入12.5g胆矾和500 mL水,配制0.1 mol·L-1的硫酸铜溶液
A.②⑤ B.①④ C.②③⑤ D.②③④⑤
(山东诸城一中2009届高三年级阶段性评估,化学,15)下列各图所示装置的气密性检查中,漏气的是
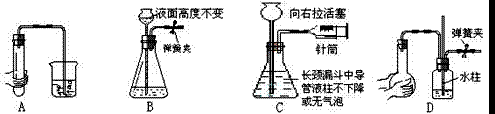 |
【巢湖市2008~2009学年高三年级第一学期期末考试】乙酸橙花酯是一种食用香料,结构如图所示。关于该物质的说法有:
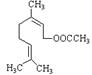
①该化合物属于酯类;②分子式C11H18O2;③1 mol该化合物最多可与2 mol H2反应;
④该化合物能发生的反应类型有:加成、取代、氧化、聚合;⑤该化合物的同分异构体可能含有苯环。其中正确的是
A.②③⑤ B.①③④ C.①④⑤ D.①③⑤
一、
题号
1
2
3
4
5
答案
A
D
C
B
C
二、
题号
6
7
8
9
10
11
12
13
14
15
16
17
答案
D
D
C
C
D
B
D
B
B
D
C
D
三、
题号
18
19
20
21
22
答案
C
AD
AC
C
BD
四、(本题共24分)
23、(每空1分,共8分)
(1)N , S
⑵ SiO2,SiO2是原子晶体,而CO2是分子晶体; H2O,水分子间作用力大于H2S分子间作用力; (3) Na2O2 (或FeS2;Na2SX等等,填写任意一个正确的即可);
(4) 
 24、(本题共8分)
24、(本题共8分)
(1) (方程式 1分,配平 1分,电子转移方向与数目 2分)
(2) SnCl2 , 3×6.02×1023 (每空1分,共2分) (3)1:1 (2分)
25、(本题共8分)
(1)放热 (1分)  (2)① 0.0175mol/L•min (1分) ②平衡(1分)
(2)① 0.0175mol/L•min (1分) ②平衡(1分)
③ 是 ,等于 ,
(每空1分,共3分) ④ a、b (2分)
五、(本题共24分)
26、(本题共12分)
(1)吸收空气中的CO2, 偏高 (每空1分,共2分)
(2)装置C反应前后质量 (1分)
(3),(5×c×v×10-3×84 )/ m1 (2分)
(4)NaHCO3(其他合理答案也可)(1分)(5)b (1分) (6)蒸发 (1分)
(7)烧杯、酒精灯 (每空1分,共2分) (8)偏高 (2分)
27、(本题共12分)
(1) 把装置中的空气赶走,防止NO被氧化为NO2 ,干燥反应中生成的气体 (每空1分,共2分) (2) 无色气体变为红棕色 ,热 (每空1分,共2分)
(3) 打开K1、K2持续通入一段时间的N2和O2 (2分)
(4)① 0.5 ②C中烧瓶在实验前后增加的质量 (每空2分,共4分)
(5)在A中加入过量含Cl-溶液,过滤后,将沉淀洗涤、干燥,最后称取沉淀的质量(2分)
(其他合理答案也可)
六、(本题共20分)
 28、(本题共8分)
28、(本题共8分)
(1)(各1分,共2分)
(2)(各1分,共2分)消去反应 酯化反应(或取代反应)
(3)(各2分,共4分)


29.(本题共12分)
(1)羟基 羧基
(各1分,共2分) (2分)
(2分)
 (2)HOCH2―CH2OH+O2
OHC―CHO+2H20 (2分) (3)B E (2分)
(2)HOCH2―CH2OH+O2
OHC―CHO+2H20 (2分) (3)B E (2分)
(4)(各2分,共4分) 
 (其他合理答案也可)
(其他合理答案也可)
七、(本题共16分)
30、(本题共6分)
(1)x=1 (2分)
(2)14.4 (2分)
(3)6 (2分)
31、(每空2分,共10分)
(1).2.8×105 ;18
(2).86.96%
(3). ;138
;138
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com