
题目列表(包括答案和解析)
(16分)
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g)
2SO3(g)
(1)此反应是工业上生产 的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 (填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
①根据有关数据,请分析在工业生产中选择常压反应器的原因:
。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g) △H= 。
2SO3(g) △H= 。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下:
①求该温度时,氨水的电离平衡常数K= 。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
① a b (填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3·H2O)= 。
(用含有a、b的式子表示)
 2SO3(g)
2SO3(g) 2SO3(g) △H= 。
2SO3(g) △H= 。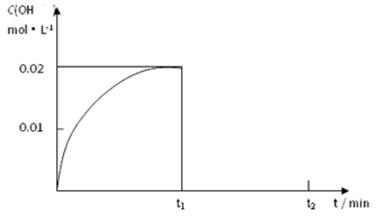
下列说法正确的是( )
| A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量。 |
| B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据。 |
| C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态。 |
| D.凡是化合反应都是放热反应,分解反应都是吸热反应。 |
下列说法正确的是( )
A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量。
B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据。
C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态。
D.凡是化合反应都是放热反应,分解反应都是吸热反应。
| A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量。 |
| B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据。 |
| C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态。 |
| D.凡是化合反应都是放热反应,分解反应都是吸热反应。 |
一.选择题(60分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
A
C
C
A
C
B
D
B
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
D
B
B
C
D
C
B
二.填空题(34分)
21.(1) 碳碳双键 氯原子 (2) 4-甲基-3-乙基辛烷
(3) 
22、  。
。
23.(1) 4 (2)_
(CH3)
24、(1) 4 。 (2) 0 个。 (3) ⑤
25.(1) 有气泡生成(1分) , 酸性高锰酸钾溶液褪色(1分) ;
(2) 除去乙烯中的乙醇,排除干扰(2分) ;
(3)  (2分); 消去反应(1分) 。
(2分); 消去反应(1分) 。
(4) D (1分)
 26、(1) 2 5
。 (2)方程式 3 H2N―C≡N
26、(1) 2 5
。 (2)方程式 3 H2N―C≡N
 ,
,
三聚氰胺的含氮量高为66.7%(1分),可提高奶粉的含氮量,冒充蛋白质(1分)
三、计算题(6分)
27、解:(1)2.3gA中含H物质的量为: =0.3mol
(1分)
=0.3mol
(1分)
由质量守恒定律可知:m有机物 + mO2 = m(CO2) + m(CO) + m(H2O)
 ×
×
2.3gA中含C物质的量为 +
+ = 0.1mol (1分)
= 0.1mol (1分)
(2) =0.05mol (1分)
=0.05mol (1分)
该有机物中C、H、O原子个数比为:2:6:1 化学式为:C2H6O (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com