(2012?信阳二模)某校化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题.
Ⅰ、探究浓硫酸的某些性质
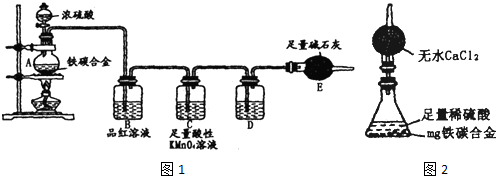
(1)按图1的连接装置,检查装置的气密性,称量E的质量.
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸.未点燃酒精灯前,A、B容器中均无明显现象,其原因是:
常温下,Fe在浓硫酸中钝化,碳不与浓硫酸反应
常温下,Fe在浓硫酸中钝化,碳不与浓硫酸反应
.
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象.写出A中发生反应的化学方程式
2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O
2Fe+6H
2SO
4(浓)
Fe
2(SO
4)
3+3SO
2↑+6H
2O
、
C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O
C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O
.
(4)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是
铁、碳在酸溶液中形成原电池
铁、碳在酸溶液中形成原电池
.
Ⅱ、测定铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重.E增重b g.则铁碳合金中铁的质量分数为
(用含m、b的表达式表示).
(6)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO
2、H
2O进入E管使b增大.你认为改进的方法是
E装置后再连接一个盛碱石灰的干燥管
E装置后再连接一个盛碱石灰的干燥管
.
(7)乙同学认为,即使甲同学认为的偏差得到改进,依据此实测得合金中铁的质量分数也可能会偏高.你认为其中的原因是
反应产生的CO2气体未能完全排到装置E中,导致b偏低
反应产生的CO2气体未能完全排到装置E中,导致b偏低
.
(8)某同学认为上述方法较复杂,使用下图所示的装置和其他常用实验仪器测定某些数据即可.为了快速准确的计算出铁的质量分数,最简便的实验操作是
C
C
(填写代号).
A.用排水法测定H
2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量.



 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.