过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:2Na
2CO
3+3H
2O
2=2Na
2CO
3?3H
2O
2△H<0
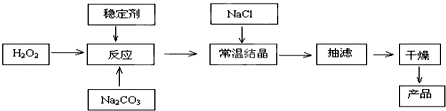
回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
强氧化性
强氧化性
.
(2)下列物质可使过碳酸钠较快失效的是
abc
abc
.
a.MnO
2 b.H
2S c.稀硫酸 d.NaHCO
3(3)加入NaCl的实验操作名称是
盐析
盐析
;作用是
降低2Na2CO3?3H2O2溶解度,析出更多晶体
降低2Na2CO3?3H2O2溶解度,析出更多晶体
.
(4)工业纯碱中含有Fe
3+等杂质,加入稳定剂的作用是与Fe
3+生成稳定的配合物,Fe
3+对反应的不良影响是
催化双氧水的分解
催化双氧水的分解
.
(5)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是
温度高时双氧水易分解
温度高时双氧水易分解
,温度偏低时造成产率低的可能是
温度低时反应缓慢
温度低时反应缓慢
.
(6)以上抽滤过程中遗漏了一步操作,造成所得产品纯度偏低,该步操作的名称是
洗涤
洗涤
;进行该操作的方法是:
向置于过滤器上的沉淀加蒸馏水至刚好淹没沉淀,静置,待水自然流出后,再重复操作两到三次
向置于过滤器上的沉淀加蒸馏水至刚好淹没沉淀,静置,待水自然流出后,再重复操作两到三次
.
(7)准确称取0.2000g 过碳酸钠样品于250mL 锥形瓶中,加50mL 蒸馏水溶解,再加50mL 2.0mol?L
-1 H
2SO
4,用2.000×10
-2 mol?L
-1 KMnO
4 标准溶液滴定至终点时消耗30.00mL,则产品中H
2O
2的质量分数为
25.50%
25.50%
.


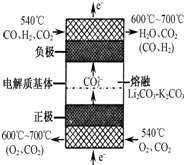
 已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
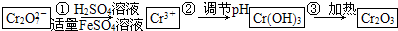
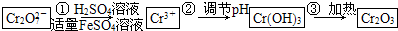
 与FeSO4溶液在酸性条件下反应的离子方程式______.
与FeSO4溶液在酸性条件下反应的离子方程式______.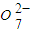 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.

