
题目列表(包括答案和解析)
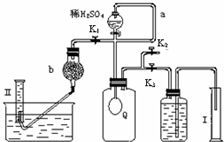 过碳酸钠(Na2CO4)在洗涤、印染、造纸、医药卫生等领域有大量应用.
过碳酸钠(Na2CO4)在洗涤、印染、造纸、医药卫生等领域有大量应用.| 12200y |
| 53x+69y |
| 12200y |
| 53x+69y |
| 17cv |
| 2ρ |
| 17cv |
| 2ρ |
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 溶液变蓝色 |
| 验证不稳定性 | 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验 |
产生气泡,木条复燃. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com