
题目列表(包括答案和解析)

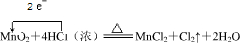
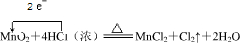
| 物质 | 室温下色、态 | 密度(g/ml) | 熔点(℃) | 沸点(℃) |
| 苯甲酸 | 白色固体 | 1.2659 | 122 | 249 |
| 甲醇 | 无色液体 | 0.7915 | -97.8 | 64.65 |
| 苯甲酸甲酯 | 无色液体 | 1.0888 | -12.3 | 199.6 |
| 乙酸 | 无色液体 | \ | 16.6 | 117.9 |
| 乙醇 | 无色液体 | \ | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | \ | 83.6 | 77.1 |

| 浓H2SO4 |
| △ |


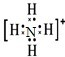
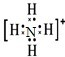
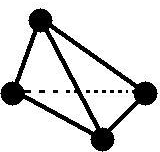

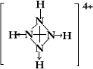

请完成下列问题:
(1)N4和N2的关系正确的是_____________(填序号)。
A.同种单质 B.同位素
C.同分异构体 D.同素异形体
(2)N4H4(SO4)2_____________(填“能”或“不能”)和草木灰混合施用。
(3)已知白磷、![]() 、
、![]() 的空间构型均为四面体,
的空间构型均为四面体,![]() 的结构式为
的结构式为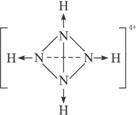 (→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
(→表示共用电子对由N原子单方面提供),白磷(P4)的结构式为![]() 。
。
请画出![]() 的结构式________________________________。
的结构式________________________________。
(4)已知液氨中存在着平衡2NH3![]()
![]() +
+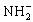 。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的
。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的![]() 生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________________________________________________。
生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com