
题目列表(包括答案和解析)
(16分)某离子化合物X由一种有机阳离子和一种无机阴离子组成;元素分析得到H:5.33%、C:21.17%、N:6.17%、S:35.33%、Ge:32.00%;该阳离子和阴离子都具有正四面体型的空间对称性。
1.确定X的组成式(阴阳离子分开写);
2.画出阴离子的空间构型;
一定条件下X能与HgI2反应,通过自组装合成了微孔硫化物Y;Y的阴离子是通过X的阴离子和HgS4变形四面体共用S形成的无限网状结构。
3.写出合成Y的反应方程式;
4.2,3-二巯基丙醇在合成Y中是不可缺少的,其可能作用是什么?
5.Y的阴离子是通过1个X中的阴离子和几个(2、3、4)Hg相连的,说明理由;
衍射法测得该晶体Y属于四方晶系,晶胞参数a=0.9269nm,c=1.4374nm,Z=2。
6.计算晶体Y的密度。
对样品进行了DSC-TG研究,在320℃附近有一个强的吸热峰,详见右图。
7.试确定残留物中的主要成分是什么?
⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 ▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为 ▲ 。在四大晶体类型中,GaN属于 ▲ 晶体。
⑵O%铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有 ▲ 的原子或离子![]()
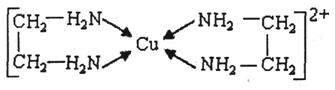
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
① H、N、O三种元素的电负性由大到小的顺序是 ▲ 。
②SO2分子的空间构型为 ▲ 。与SnCl4互为等电子体的一种离子的化学式为 ▲
③乙二胺分子中氮原子轨道的杂化类型为 ▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 ▲ 。
④⑶中所形成的配离子中含有的化学键类型有 ▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
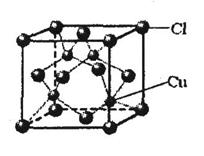
⑤CuCl的晶胞结构如右图所示,其中Cl原子的配位数为 ▲ 。
⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 ▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为 ▲ 。在四大晶体类型中,GaN属于 ▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有 ▲ 的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
① H、N、O三种元素的电负性由大到小的顺序是 ▲ 。
②SO2分子的空间构型为 ▲ 。与SnCl4互为等电子体的一种离子的化学式为 ▲
③乙二胺分子中氮原子轨道的杂化类型为 ▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 ▲ 。
④⑶中所形成的配离子中含有的化学键类型有 ▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
⑤CuCl的晶胞结构如右图所示,其中Cl原子的配位数为 ▲ 。
(10分)
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转换关系,已知C为密度最小的气体,甲是电解质。
根据图示转化关系回答:
(1)写出下列物质的化学式:B 、丙 、丁 。
(2)组成单质A的元素在周期表中的位置是 。
(3)乙与过量CO2反应的离子方程式____________________________。
(12分)⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 ▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为 ▲ 。在四大晶体类型中,GaN属于 ▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有 ▲ 的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
① H、N、O三种元素的电负性由大到小的顺序是 ▲ 。
②SO2分子的空间构型为 ▲ 。与SnCl4互为等电子体的一种离子的化学式为 ▲
③乙二胺分子中氮原子轨道的杂化类型为 ▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 ▲ 。
④⑶中所形成的配离子中含有的化学键类型有 ▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com