
题目列表(包括答案和解析)
下列方程式中正确的是
A.碳酸钠的水解方程式: 2H2O+CO32- ![]() H2CO3+2OH-
H2CO3+2OH-
B.碳酸氢钠在水溶液中的电离:NaHCO3 ![]() Na+ + H+ + CO32-
Na+ + H+ + CO32-
C.醋酸的电离方程式:CH3COOH + H2O ![]() CH3COO- + H3O+
CH3COO- + H3O+
D.氢硫酸的电离方程式: H2S ![]() 2H++S2-
2H++S2-
下列离子方程式错误的是
A.氯气通入水中:C12 + H2O![]() H+ + C1- + HClO
H+ + C1- + HClO
B.向3%的双氧水中通入少量SO2:H2O2 + SO2 = 2H+ + SO42―
C.碳酸钠水解:CO32― + 2H2O = H2CO3 + 2OH-
D.向NaHCO3溶液中加入过量石灰水:Ca2++OH-+ HCO3- = CaCO3↓+H2O
下列离子方程式错误的是
A.氯气通入水中:C12 + H2O 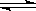 H+ + C1-+ HClO
H+ + C1-+ HClO
B.向3%的双氧水中通入少量SO2:H2O2 + SO2 === 2H+ + SO42-
C.碳酸钠水解:CO32- + 2H2O 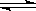 H2CO3 + 2OH-
H2CO3 + 2OH-
D.向NaHCO3溶液中加入过量石灰水:Ca2+ + OH-+ HCO3-== CaCO3↓+ H2O
A.氯气通入水中:C12 + H2O H+ + C1-+ HClO H+ + C1-+ HClO |
| B.向3%的双氧水中通入少量SO2:H2O2 + SO2= 2H+ + SO42― |
| C.碳酸钠水解:CO32―+ 2H2O= H2CO3 + 2OH- |
| D.向NaHCO3溶液中加入过量石灰水:Ca2++OH-+ HCO3- = CaCO3↓+H2O |
 H+ + Cl- + HClO
H+ + Cl- + HClO 第Ⅰ卷(选择题 共42分)
一、选择题(本题包括14小题,每小题3分,共42分,每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
答案
C
B
C
B
C
A
B
题号
8
9
10
11
12
13
14
答案
C
A
C
D
B
A
C
第Ⅱ卷(共58分)
二、填空题(本题包括4小题,共48分)
15.(13分)
(1)①增大(1分)
②增大 减小(各1分,共2分)
③E(1分)
④t3~t5(1分)
⑤D B(各1分,共2分)
⑥
(2)2NH3+60H--6e-===N2+6H2O(2分) 碱性(1分)
NH3在酸性介质中易转化为NH4+离子(1分)
16.(12分)
(1)第二周期 第VA族(各0.5分共1分)
(2)NH3+H+===NH4+(或H2O+H+===H3O+)(2分)
(3)Al3++3H2O Al(OH)3+3H+(2分)
Al(OH)3+3H+(2分)
(4)NaOH; NH4NO3(各1分共2分)
(5)2H2-4e-+4OH===4H2O(2分)
(6)①A(1分)
②0.25mol2?L-2(或0.25)(2分)
17.(9分)
(1)①吸收CO2中的水蒸汽(或干燥CO2气体)(1分)
②防止空气中的二氧化碳和水蒸汽进入C中(1分)
③C(1分)
(2)①NaOH溶液(1分)
②过滤(1分) 干燥(1分)
③ (2分)
(2分)
(3)方案一中的CO2气体不能完全被装置C中的碱石灰吸收(1分)
18.(14分)
(1)离子键、共价键(或非极性键)(各0.5分共1分)
0.2NA 或1.024×1023 (1分)
(2)Cl2+2OH-===Cl- + ClO- +H2O(2分)
(3)C+2H2SO4(浓)△CO2↑+2SO2↑+2H2O(2分)
(4)NH4++HCO3-+2OH-△NH3↑+CO32-+2H2O(2分)
(或:NH4++HSO3-+2OH-△NH3↑+SO32-+2H2O,
(或:NH4++HS-+2OH-△NH3↑+S2-+2H2O,其它正确答案亦可)
(5)4HCl+NaAlO2===NaCl+AlCl3+2H2O(2分)
(或:4H2SO4+2NaAlO2===Na2SO4+Al2(SO4)3+4H2O,若H2SO4写成硝酸亦可)
(6)2NH4Cl+Ca(OH)2△CaCl2 +2H2O+2NH3↑(2分)
4NH3(g)+5O2(g)===4NO(g)+6H2O(g);△H=-906.8KJ/mol(2分)
三、选做题(本题分A、B两题,考生只要选其中一题作答。若两题都作答,则以A题得分计入总分。本题共10分)
(1)Na<Al<Si<N 高
(2)高 NaCl为离子晶体而SiCl4为分子晶体
(3)三角锥形
(4)1s22s22p63s23p63d104s1(或[Ar] 3d104s1) [Cu(NH3)4]2+
(5)Cu3 N
(6)AlN 共价键
19B.(各1分共10分)
(I)
(II)(1)加成反应 消去反应
(2)浓硫酸、加热
(3) 

(4) 银氨溶液[或新制Cu(OH)2悬浊液]
银氨溶液[或新制Cu(OH)2悬浊液]
(5)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com