
题目列表(包括答案和解析)
一定温度和压强下N2+3H2![]() 2NH3反应达到平衡后,下列说法中正确的是
2NH3反应达到平衡后,下列说法中正确的是
A.N2与H2不再化合,NH3不再分解
B.N2、H2化合成氨的反应速率等于NH3 分解的反应速率
C.H2、NH3的体积分数相等
D.N2、H2、NH3的物质的量浓度相等
| | N2+3H2 2NH3 2NH3 | |||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
(10分)已知:合成氨反应为N2+3H2![]() 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系 (填“I”“II”“III”)
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为 (填“A”“B”“C”“D”)
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =
(10分)已知:合成氨反应为N2+3H2 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系 (填“I”“II”“III”)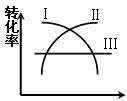
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为 (填“A”“B”“C”“D”)
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =
 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:

1.C 2.D 3.CD 4.C 5.AC 6.AD 7.C 8.A 9.D 10.C 11.AB 12.A
13.B 14.D 15.B 16.B 17.BC 18.B
19.(1)NaOH;HClO4;Al(OH)3 (2)Ne;F;F2;Na (3)HF; (4)Na
阶段测试卷(A卷).files/image015.gif)
阶段测试卷(A卷).files/image016.gif)
阶段测试卷(A卷).files/image017.gif) 20. (1)D (2) 因原电池反应,铜将在银棒(正极)上析出而不是在铁棒上,所以应该是银棒下沉铁棒上升.
20. (1)D (2) 因原电池反应,铜将在银棒(正极)上析出而不是在铁棒上,所以应该是银棒下沉铁棒上升.
21.(1) ;离子键 (2)两种;
(3)复分解反应 (4)<
22.(1)△H =-92kJ/mol (2)△H=-30.6 kJ/mol
阶段测试卷(A卷).files/image018.gif)
阶段测试卷(A卷).files/image019.gif) 23. ⑴ N
③; ⑵ Sn
④; ⑶ Fe
①
23. ⑴ N
③; ⑵ Sn
④; ⑶ Fe
①
24.(1)NH4+;OH-; H2O ; NH3 (2)NH4+ + OH-== NH3 + H2O
25.O N S H
26. 呈现红色的部位发生了2H++2e = H2,而导致H+浓度下降,致使[OH-]>[H+],所以A是负极,B是正极
27. (1)v0=2.73×10-8 mol/(L•s)
(2)当I2消耗一半时,
c(CH3COCH3)=0.1mol/L―1/2×0.01mol/L=0.095mol/L,
c(H+)=0.1mol/L+1/2×0.01mol/L=0.015mol/L,此时的反应速率vt=2.73×10-5×0.095×0.015mol/(L•s)=3.89×10-8 mol/(L•s)显然 vt >
v0,所以反应速率比开始时快阶段测试卷(A卷).files/image014.jpg)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com