
题目列表(包括答案和解析)
亚氯酸钠(NaClO2)可用作漂白剂,在酸性溶液中生成HClO2而发生分解,分解的化学方程式为2HClO2=2ClO2↑+HClO+H2O,ClO2是广谱消毒剂。下列说法正确的是( )
A.上述反应中,氧化剂与还原剂物质的量之比1:2
B.上述反应中,ClO2是还原产物
C.上述反应中,1molHClO2分解转移2mol电子
D.HClO2是有机酸
亚氯酸钠(NaClO2)可用作漂白剂,在酸性溶液中因生成亚氯酸而发生分解,分解的化学方程式为5HClO2 = 4ClO2↑+ HCl + 2H2O,ClO2是广谱型消毒剂。下列说法正确的是( )
A.HClO2是有机酸
B.上述反应中,ClO2是还原产物
C.上述反应中,1 mol HClO2分解转移2 mol电子
D.上述反应中,氧化剂与还原剂物质的量之比为1:4
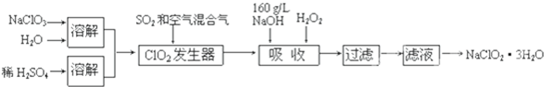
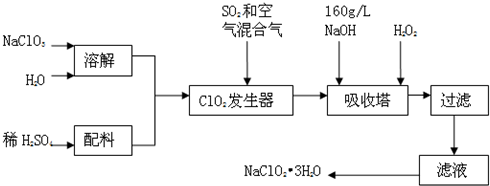
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体只能保持在稀释状态下以防止爆炸性分解,且需现合成现用。
③ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式: 。
(2)反应生成ClO2气体需要X酸酸化的原因为: 。X酸为 。
(3)吸收塔内的温度不能过高的原因为:
(4)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为ClO2—或Cl—。ClO2被S2—还原为ClO2—、Cl—的转化率与溶液pH的关系如右图所示。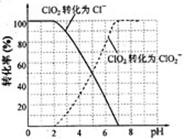
请写出pH≤2时ClO2与S2—反应的离子方程式: 。
(5)第二步向NaClO3溶液中通SO2的同时通入空气的原因为: 。
(6)从滤液中得到NaClO2●3H2O粗晶体的操作步骤为
、 、 。
1D
26.(1) H;
(2)2Mg + CO2 = 2MgO + C
(3)Na2CO3
(4)H
27.(1)CaC2+2H2O→Ca(OH)2+C2H2↑, 
(2)4
(3)棕黄色溶液变无色或褪色; 4.8
(4)合成氨原料,作燃料或有机化工原料(其他合理答案均给分)
28.(每空2分,共16分)
(1) 
(2)4Fe + 3 O2 +2 x H2O === 2 Fe2O3•x H2O
(3)2 FeCl3 + Fe == 3 FeCl2
(4)B D
(5)① 铜 Cu2+ + 2e- == Cu
② 0.08 mol
③ 铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀。(其他答案合理也给分)
29.(1)(4分)第三周期,第IA族; 
(2)(2分)2 NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(3)(6分)ClO―+ H2O  HClO +OH―
HClO +OH―
I、ClO―+Cl―+2H+ =Cl2↑+ H2O II、在a、b装置之间加一盛有饱和食盐水(或水)的洗气瓶,除去HCl
(4)(3分)3 mol ≤n(e―)≤5 mol
30.(
(2) n平(NH3)= ×25%=32 mol×25%=8 mol
×25%=32 mol×25%=8 mol
(2) 5∶4
(3) 2∶3
(4) 1∶2
(5) 3∶3∶2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com