
题目列表(包括答案和解析)
下列图示与对应的叙述相符的是

A.图I表示向1L浓度均为0.1 mol/L的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol/L稀H2SO4溶液,产生沉淀量的变化
B.图Ⅱ中逆反应的热效应△H=E1- E2 <0,所以逆反应为放热反应
C.图Ⅲ表示向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液,溶液pH的变化,c点溶液中:c(HCO3一)+2c(CO32一)+c(C1-)>c(Na+)
D.用0.1 mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图Ⅳ曲线可确定HX的酸性最强

| A.图I表示向1L浓度均为0.1 mol/L的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol/L稀H2SO4溶液,产生沉淀量的变化 |
| B.图Ⅱ中逆反应的热效应△H=E1- E2 <0,所以逆反应为放热反应 |
| C.图Ⅲ表示向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液,溶液pH的变化,c点溶液中:c(HCO3一)+2c(CO32一)+c(C1-)>c(Na+) |
| D.用0.1 mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图Ⅳ曲线可确定HX的酸性最强 |
下列图示与对应的叙述相符的是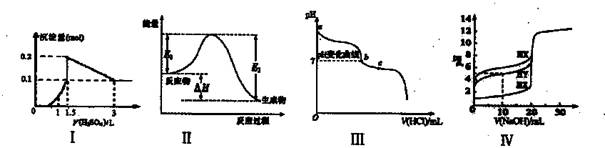
| A.图I表示向1L浓度均为0.1 mol/L的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol/L稀H2SO4溶液,产生沉淀量的变化 |
| B.图Ⅱ中逆反应的热效应△H=E1- E2 <0,所以逆反应为放热反应 |
| C.图Ⅲ表示向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液,溶液pH的变化,c点溶液中:c(HCO3一)+2c(CO32一)+c(C1-)>c(Na+) |
| D.用0.1 mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图Ⅳ曲线可确定HX的酸性最强 |
下列说法正确的是
| A.室温下,pH之和为14的氨水与盐酸等体积混合,溶液一定呈中性 |
| B.在0.1 mol/L(NH4)2Fe(SO4)2溶液中[来源:学.科.网] c(H+)+c(NH4+)+2c(Fe2+)=c(OH-)+c(SO42-) |
| C.向醋酸溶液中加入适量醋酸钠,所得酸性溶液中 c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.0.4 mol/L HCl与0.1 mol/L NaAlO2等体积混合,所得溶液中: |
1D
26.(1) H;
(2)2Mg + CO2 = 2MgO + C
(3)Na2CO3
(4)H
27.(1)CaC2+2H2O→Ca(OH)2+C2H2↑, 
(2)4
(3)棕黄色溶液变无色或褪色; 4.8
(4)合成氨原料,作燃料或有机化工原料(其他合理答案均给分)
28.(每空2分,共16分)
(1) 
(2)4Fe + 3 O2 +2 x H2O === 2 Fe2O3•x H2O
(3)2 FeCl3 + Fe == 3 FeCl2
(4)B D
(5)① 铜 Cu2+ + 2e- == Cu
② 0.08 mol
③ 铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀。(其他答案合理也给分)
29.(1)(4分)第三周期,第IA族; 
(2)(2分)2 NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(3)(6分)ClO―+ H2O  HClO +OH―
HClO +OH―
I、ClO―+Cl―+2H+ =Cl2↑+ H2O II、在a、b装置之间加一盛有饱和食盐水(或水)的洗气瓶,除去HCl
(4)(3分)3 mol ≤n(e―)≤5 mol
30.(
(2) n平(NH3)= ×25%=32 mol×25%=8 mol
×25%=32 mol×25%=8 mol
(2) 5∶4
(3) 2∶3
(4) 1∶2
(5) 3∶3∶2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com