
题目列表(包括答案和解析)
|
下列物质间反应的离子方程式正确的是 | |
| [ ] | |
A. |
相同物质的量浓度的FeI2溶液与溴水等体积混合2Fe2++2I-+2Br2=2Fe3+I2+4Br2- |
B. |
Ba(OH)2溶液中加入过量的NaHSO4溶液Ba2++OH-+H++SO42-=BaSO4↓+H2O |
C. |
四氧化三铁溶于氢碘酸溶液中Fe3O4+8H++2I-=3Fe2++I2+4H2O |
D. |
向漂白粉溶液中加入适量的SO2 Ca2+2ClO-+SO2+H2O=CaSO3↓+2HClO |
 有些化学反应的化学能能直接转化成电能
有些化学反应的化学能能直接转化成电能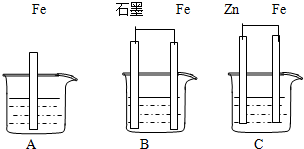
| 放电 | 充电 |
(10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值,其实验方案的要点为:
①用直流电电解氯化铜溶液,所用仪器如图:
②在电流为I A,通电时间为t s后,精确测得某电极上析出的铜的质量为m g.
试回答:
(1)连接这些仪器的正确顺序为:(用图中标注仪器接线柱的英文字母表示,下同)E接________,C接________,________接F.
(2)写出B电极上发生反应的离子方程式________________.G试管中淀粉KI溶液变化的现象为__________________,相应的离子方程式是__________________.
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序是________.(选填下列操作步骤的编号)
①称量电解前电极质量
②刮下电解后电极上的铜并清洗
③用蒸馏水清洗电解后电极
④低温烘干电极后称量
⑤低温烘干刮下的铜后称量
⑥再次低温烘干后称量至恒重
(4)已知电子的电荷量为1.6×10-19C.试列出阿伏伽德罗常数的计算表达式:NA=________.
第Ⅰ卷(选择题,共45分)
1. D 2.C 3.C 4.D 5.C 6.D 7.C 8.B 9.B 10.C
11.D 12.A 13.D 14.D 15.D
第Ⅱ卷 (非选择题,共55分)
16.(10分)(1)KIO3(2分);淀粉溶液(2分)。
(2)4KI+02+2H20 → 2I2 + 4KOH(只要能表示出KI、02和I2即可得分,不配平不扣分)
(2分)
(3)C→B→D→A→G→H→E→F(2分)
使漏斗下端管壁紧靠烧杯内壁;及时关闭活塞,不要让上层液体流出。(2分)
17.(13分)(1)空气污染、酸雨(2分);2S02+ 02 =2S03
SO3+H20=H2SO4(或SO2+H2O=H2SO3 2H2SO3+02=2H2SO4)(4分)
(2)CaCO3+SO2=CaSO3+CO2↑ 2CaSO3+O2=2CaSO4(4分)
(3)CaO [或石灰石均可得分](3分)
18.(16分)(1)关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,若活塞能回到原位,证明不漏气,否则漏气。(4分)
(2)偏小(1分),将广口瓶中的水改为饱和CO2水溶液(或在水面上覆盖一层植物油等)
(2分)。
(3)Ⅰ没有吸收圆底烧瓶水蒸汽的装置;Ⅱ球形干燥管与空气相通;Ⅲ反应结束后,装置内残留的C02不能完全排出。(其他合理答案可酌情给分)(3分)
(4)过滤(或过滤洗涤)(1分);干燥(或烘干)(1分)。
静置,在上层清液中继续滴加CaCl2溶液,若无沉淀证明沉淀已完全。(2分)
(5)  (2分)
(2分)
19.(16分)
(2)放热(1分);放出氧气(1分)。
(3)I可能CO2过量,瓶中02少,CO2多(1分)。 3(1分)。
Ⅱ发烫(1分)。 2(1分)。
Ⅲ塞上带导管的橡皮塞(2分),澄清石灰水(1分)。澄清石灰水变浑浊(1分)。 1(1分)。
(4) Na2O2部分变质或滴入的水太多(2分);生成的NaOH使酚酞变红,但Na2O2或
H202具有强氧化性,将酚酞氧化而漂白。(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com