
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ёщҫЭПВБРЧ°ЦГНј»ШҙрОКМвЎЈ
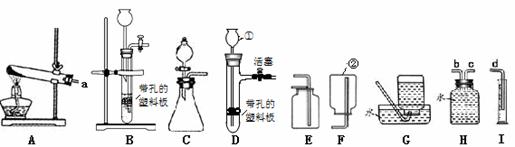
ўс.РҙіцТЗЖчўЩөДГыіЖКЗ ўМ Ј¬ТЗЖчўЪөДГыіЖ ўН ЎЈ
ўт.КөСйКТУГТ»¶ЁЦКБҝөДВИ ЛбјШЦЖИЎСхЖшЈ¬НЁ№эЕЕЛ®БҝІв¶ЁЛщКХјҜөҪөДСхЖшМе»эЎЈ
ЛбјШЦЖИЎСхЖшЈ¬НЁ№эЕЕЛ®БҝІв¶ЁЛщКХјҜөҪөДСхЖшМе»эЎЈ
ўЩРҙіцёГ·ҙУҰөД»ҜС§·ҪіМКҪ ўО ЎЈ
ўЪИфёчЧ°ЦГөДБ¬ҪУЛіРтКЗЈәaЎъbЎъcЎъdЈ¬HЧ°ЦГДЪөј№ЬЈЁЎ°bЎұ»тЎ°cЎұЈ©ёГФхСщСУЙмЈҝЗл»ӯіцўП ЎЈ
ўЫёщҫЭВИЛбјШөДЦКБҝЛгіцөДСхЖшМе»эОӘАнВЫЦөЈ®Из№ыКөјКІвөГСхЖшөДМе»эҙуУЪАнВЫЦөЈЁЛ®өДМе»эІвБҝЧјИ·Ј©Ј¬ДгИПОӘФӯТтКЗ ўР ЎЈ
ўу.ДіРЛИӨРЎЧйОӘБЛСЎФсКөСйКТЦЖИЎ¶юСх»ҜМјөДФӯБПЈ¬¶ФУ°ПмСОЛбУлҙуАнКҜЈЁҙуАнКҜЦРФУЦКІ»УлСОЛб·ҙУҰЈ©·ҙУҰөДЛЩВКҝмВэөДТтЛШХ№ҝӘСРҫҝЎЈ
МбіцјЩЙиЈәСОЛбУлҙуАнКҜ·ҙУҰөДЛЩВКҝмВэУлЛщУГHClөДЦКБҝ·ЦКэЎўҙуАнКҜҝЕБЈҙуРЎУР№ШЎЈ
КөСйЙијЖУлКөК©Јә
| КөСйұаәЕ | ОВ¶И | 5ҝЛҙуАнКҜЈЁМјЛбёЖҙҝ¶ИПаН¬Ј©№жёс | 20ҝЛHClөДЦКБҝ·ЦКэ | НкИ«·ҙУҰЛщРиКұјд/s |
| КөСйўЩ | 20Ўж | ҙЦҝЕБЈ | 20% | 140 |
| КөСйўЪ | 20Ўж | ҙЦҝЕБЈ | 10% | 220 |
| КөСйўЫ | 20Ўж | ПёҝЕБЈ | 20% | 30 |
ёщҫЭТФЙПРЕПў»ШҙрПВБРОКМвЈә
РҙіцЙПКцКөСйЦР·ҙУҰөД»ҜС§·ҪіМКҪ ўС ЎЈ
КөСйўЩУлўЪөДДҝөДКЗОӘБЛМҪҫҝ ўТ ЎЈ
КөСй ўУ ЈЁМоКөСйұаәЕЈ©өДДҝөДКЗОӘБЛМҪҫҝҙуАнКҜҝЕБЈҙЦЎўПё¶Ф·ҙУҰҝмВэөДУ°ПмЎЈ
КөСйҪбВЫЈәHClЦКБҝ·ЦКэФҪҙуЈ¬·ҙУҰФҪҝмЈ»№ММеөДҝЕБЈФҪРЎЈ¬·ҙУҰФҪҝмЎЈ
НШХ№Ул·ҙЛјЈә»№УРДДР©ТтЛШҝЙДЬУ°ПмёГ·ҙУҰөДЛЩВКҝмВэДШЈҝЗлРҙіцДгөДТ»ёцІВПлЈә ўФ ЎЈ
ёщҫЭЙПКцКөСйМҪҫҝЈ¬КөСйКТСЎУГҝйЧҙҙуАнКҜУлПЎСОЛбЦЖИЎ¶юСх»ҜМјЈ¬СЎУГЙПНјЦРҫЯУРЖфЖХ·ўЙъЖчФӯАн өД ўХ ЈЁМоұаәЕЈ©Ч°ЦГЧчОӘЦЖИЎ¶юСх»ҜМјөД·ўЙъЧ°ЦГЎЈ
өД ўХ ЈЁМоұаәЕЈ©Ч°ЦГЧчОӘЦЖИЎ¶юСх»ҜМјөД·ўЙъЧ°ЦГЎЈ
ўф.КөСйКТФЪіЈОВПВУГҝйЧҙөзКҜ№ММеУлЛ®·ҙУҰЦЖИЎТТИІЖшМеЈ¬ ёГ·ҙУҰұШРлСПёсҝШЦЖјУЛ®ЛЩ¶ИЈ¬ТФГвҫзБТ·ҙУҰТэЖр·ўЙъЧ°ЦГХЁБСЈ»ТТИІКЗТ»ЦЦОўИЬУЪЛ®ЗТГЬ¶ИұИҝХЖшВФРЎөДЖшМеЎЈЙПНјЦРЦЖИЎҪПҙҝТТИІөДЧоККТЛ·ўЙъәНКХјҜЧ°ЦГКЗ ўЦ ЈЁМоұаәЕЈ¬іэЧ°ЦГHәНIНвЈ©ЎЈ
ёГ·ҙУҰұШРлСПёсҝШЦЖјУЛ®ЛЩ¶ИЈ¬ТФГвҫзБТ·ҙУҰТэЖр·ўЙъЧ°ЦГХЁБСЈ»ТТИІКЗТ»ЦЦОўИЬУЪЛ®ЗТГЬ¶ИұИҝХЖшВФРЎөДЖшМеЎЈЙПНјЦРЦЖИЎҪПҙҝТТИІөДЧоККТЛ·ўЙъәНКХјҜЧ°ЦГКЗ ўЦ ЈЁМоұаәЕЈ¬іэЧ°ЦГHәНIНвЈ©ЎЈ

| ||
| ||
| ||
| ||
ЈЁ10·ЦЈ©ЗлёщҫЭПВБРКөСйЧ°ЦГНј»ШҙрУР№ШОКМвЈә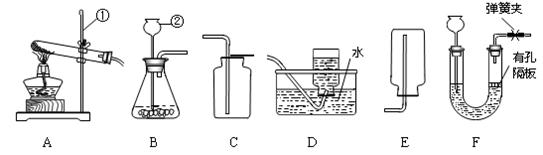
ЈЁ1Ј©ЗлРҙіцұкәЕТЗЖчөДГыіЖЈәўЩ Ј¬ўЪ ЎЈ
ЈЁ2Ј©КөСйКТСЎУГBЎўDЧ°ЦГЦЖИЎO2Ј¬·ҙУҰөД»ҜС§·ҪіМКҪКЗ Ј»
ЈЁ3Ј©СЎФс·ўЙъЧ°ЦГBәНКХјҜЧ°ЦГ ЈЁСЎМоРтәЕЈ©ҝЙУГУЪКөСйКТЦЖИЎҪПОӘёЙФпөДCO2Ј¬¶ФУҰөД»ҜС§·ҪіМКҪКЗ Ј»ИфҪ«·ўЙъЧ°ЦГУЙBёДОӘFЈ¬ЖдУЕөгКЗ ЎЈИфҪ«КХјҜЧ°ЦГёДУГПВНјGЛщКҫТҪУГЛЬБПҙьЈ¬ФтЖшМеөјИл¶ЛОӘ ЈЁМоЎ°aЎұ»тЎ°bЎұЈ©ЎЈ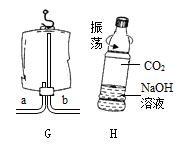
ЈЁ4Ј©УГЙПНјHЛщКҫөДҝуИӘЛ®ЖҝҪшРР¶ФұИКөСйЈ¬ҝЙТФЦӨГчCO2УлNaOHИЬТәИ·Кө·ўЙъБЛ·ҙУҰЈ¬УҰЧцөД¶ФұИКФСйКЗ ЎЈ
ЗлёщҫЭПВБРЧ°ЦГЈ¬»ШҙрОКМвЈә
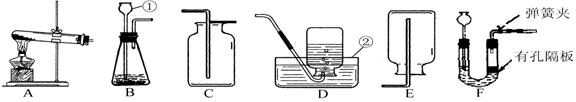
 |
ЈЁ1Ј©РҙіцұкәЕўЩәНўЪөДТЗЖчГыіЖ ЎЈ
ЈЁ2Ј©Ч°ЦГBЦРТЗЖчўЩөДПВ¶Л№ЬҝЪТӘҪюФЪТәГжПВЈ¬КЗОӘБЛ ЎЈ
ЈЁ3Ј©КөСйКТјУИИ°өЧПЙ«№ММеЦЖИЎO2өД·ҙУҰ·ыәЕұнҙпКҪОӘ Ј¬ИфУГЕЕЛ®·ЁКХјҜЖшМеЈ¬өұ№ЫІмөҪ_____ ___КұІЕҝӘКјКХјҜЈ»НЈЦ№КөСйКұЈ¬УҰёГ_____ _____ _Ј¬·сФт_______________ ____________ЎЈ
ЈЁ4Ј©ИфУГЧ°ЦГCЎўD»тKКХјҜO2Ј¬ТӘК№КХјҜO2ёЙФпЗТҙҝҫ»Ј¬ФтУҰСЎ Ч°ЦГЎЈИфУГЕЕЛ®·ЁКХјҜөҪөДO2І»ҙҝЈ¬ҝЙДЬөДФӯТтКЗЈҝЈЁБҪМхЈ©_____________ ____________Ўў_________________ ___________ЎЈ
ИфУГПтЙПЕЕҝХЖш·ЁКХјҜСхЖшЈ¬ИзәОСйВъЈҝ_________ ____________ _________ЎЈ
КөСй№эіМЦР·ўПЦЛ®ІЫЦРөДЛ®ұдіЙБЛЗіЧПәмЙ«Ј¬ҝЙДЬөДІЩЧчФӯТтЈә_____ ___________ ЎЈ
ЈЁ5Ј©УГ№эСх»ҜЗвИЬТәУл¶юСх»ҜГМЦЖИЎO2Ј¬Ч°ЦГGЛдИ»ІЩЧчјтұгЈ¬ө«ТӘөГөҪЖҪОИөДЖшБчЈ¬ҙУHЎўIЎўJЦРСЎИЎЎЎ ЎЎИЎҙъGЦРөДөҘҝЧИыЈ¬ТФҙпөҪДҝөДЎЈИфСЎУГHУлЧ¶РОЖҝЧйЧ°өД·ўЙъЧ°ЦГЈ¬өұ·ҙУҰНЈЦ№КұЈ¬јҜЖшЖҝЦР»№ІоЙЩБҝO2Ј¬ОӘјҜВъO2Ј¬ФЪІ»ІрР¶Ч°ЦГөДЗ°МбПВЈ¬ҝЙТФ Ўў
ЎЈКөСйҪбКшәуЈ¬ёГН¬С§·ўПЦКХјҜөҪөДЖшМеұИФӨјЖөДЙЩәЬ¶аЈ¬°ЩЛјІ»өГЖдҪвЎЈДгИПОӘҝЙДЬөДФӯТтКЗЈә___________ ___ _________ЎЈ
ЈЁ6Ј©¶ФУГВИЛбјШәН¶юСх»ҜГМөД»мәПОпЦЖИЎO2әуөД№ММеІРФьЈЁјЩ¶ЁТСНкИ«·ҙУҰЈ©Ј¬НЁ№эТФПВЛДІҪКөСйІЩЧчҝЙ»ШКХ¶юСх»ҜГМЎЈХэИ·ІЩЧчөДПИәуЛіРтКЗ ЈЁМоРҙСЎПоРтәЕЈ©ЎЈ
aЈ®әжёЙ bЈ®ИЬҪв cЈ®№эВЛ dЈ®ПҙөУ
ЈЁ7Ј©КөСйКТАыУГFЧ°ЦГЦЖұёЗвЖшЈ¬КВПИҪ«РҝБЈ·ЕУЪУРҝЧёф°еЦ®ЙПЈ¬И»әуҙУБнТ»¶ЛјУИлПЎСОЛбЈ¬Ч°ЦГFПа¶ФУЪЧ°ЦГBЦЖұёЗвЖшЈ¬ҫЯУРөДУЕөгКЗ ЎЈИфУГLЧ°ЦГКХјҜЗвЖшЈ¬ФтЖшМеҙУ ¶ЛНЁИлЈЁМоЎ°aЎұ»тЎ°bЎұЈ¬ПВН¬Ј©Ј»ИфТӘҪ«LЧ°ЦГЦРөДЗвЖшУГЛ®ЕЕіцЈ¬ФтЛ®ҙУ ¶ЛНЁИлЎЈ
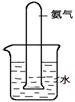 ЈЁ8Ј©ІйФДЧКБПЈәКөСйКТіЈУГјУИИВИ»Ҝп§ЈЁNH4ClЈ©әНКмКҜ»Т[Ca(OH)2]БҪЦЦ№ММе»мәПОп
ЈЁ8Ј©ІйФДЧКБПЈәКөСйКТіЈУГјУИИВИ»Ҝп§ЈЁNH4ClЈ©әНКмКҜ»Т[Ca(OH)2]БҪЦЦ№ММе»мәПОп
өД·Ҫ·ЁЦЖИЎ°ұЖшЈЁNH3Ј©Ј¬Н¬Кұ»№ЙъіЙВИ»ҜёЖЈЁCaCl2Ј©әНЛ®Ј¬ФтёГ·ҙУҰөД·ыәЕұнҙпКҪОӘ
Ј»БнНвЈ¬°ұЖшУРҙМјӨРФЖшО¶ЗТј«ТЧИЬУЪЛ®Ј¬ФтФЪ
КөСйКТАп°ұЖшөДЦЖИЎЧ°ЦГКЗ_________ЎЈРЎҫьЙијЖБЛИзНјЛщКҫөДТ»ёцКөСйЈәідВъ°ұЖшөД
Т»Ц§КФ№Ьө№ЦГУЪТ»ёцЧ°УРЧгБҝЛ®өДЙХұӯЦРЎЈТ»¶ОКұјдәуЈ¬Ҫ«»бҝҙөҪЈә ЎЈ
ЈЁ9Ј©Ді»ҜѧСЧйФЪС§П°БЛЦЖИЎO2әуЈ¬ЛыГЗ·ўПЦФЪКөСйКТАпУГ5% H2O2ИЬТәјУИИЦЖO2Ј¬УГҙш»рРЗөДДҫМхјмСйЈ¬ДҫМхәЬДСёҙИјЎЈН¬С§ГЗҫӯ№эИПХж№ЫІмЈ¬ІВПлЖдҝЙДЬФӯТтКЗ ЎЈ
ОӘБЛСйЦӨҙЛІВПлКЗ·сХэИ·Ј¬РЛИӨРЎЧйөДН¬С§ҫӯ№эИИБТМЦВЫЈ¬ЦЖ¶ЁБЛКөСй·Ҫ°ёІўҪшРРБЛКөСйЎЈ
өЪТ»ЧйН¬С§ІЙИЎФцҙуH2O2ИЬТәЕЁ¶ИөД·Ҫ·ЁЈ¬УГ10%өДH2O2ИЬТәјУИИЈ¬
 Т»¶ОКұјдәуЈ¬УГҙш»рРЗөДДҫМхјмСйЈ¬ДҫМхёҙИјЈ»
Т»¶ОКұјдәуЈ¬УГҙш»рРЗөДДҫМхјмСйЈ¬ДҫМхёҙИјЈ»
өЪ¶юЧйН¬С§ФЪ5%өДH2O2ИЬТәЦРјУИл2өОРВЦЖЗвСх»ҜДЖИЬТәЈ¬јУИИ
Т»¶ОКұјдәуЈ¬УГҙш»рРЗДҫМхјмСйЈ¬ДҫМхёҙИјЈ»
өЪИэЧйН¬С§ҙУКөСйЧ°ЦГЙПҪшРРБЛёДҪшЈ¬Р§№ыәЬәГЈЁјыНјЈ©ЎЈ
ФЪКөСй»щҙЎЙПЈ¬Н¬С§ГЗҫӯ№эҪ»БчМЦВЫЈ¬өГіцБЛТ»Р©ҪбВЫЈә
ўЩУЙөЪТ»ЧйКөСйҝЙөГіцУ°ПмH2O2·ЦҪвІъЙъO2¶аЙЩј°ҝмВэөДТтЛШЦ®Т»КЗ Ј»
ўЪУЙөЪ¶юЧйКөСйҝЙ·ЦОцөГіцЗвСх»ҜДЖЛщЖрөДЧчУГҝЙДЬКЗ Ј»
ўЫөЪИэЧйКөСйСйЦӨБЛКөСйЗ°Н¬С§ГЗІВПлөДХэИ·РФЎЈЖдЦРЕЁБтЛбөДЧчУГКЗ Ј»
ўЬРЎАоН¬С§ИПХж№ЫІмБЛөЪИэЧйН¬С§өДКөСйЧ°ЦГЈ¬МбіцБЛТ»ЦЦјтөҘөДёДҪшЧ°ЦГЈ¬ҫӯПЦіЎКөСйЈ¬Р§№ыәЬәГЈ¬ЗлДгЛөіцЛыёДҪшөДөШ·ҪЈә ЎЈ


Т»Ј®өҘПоСЎФсМвЈЁГҝРЎМв3·ЦЈ¬№І36·ЦЈ©
1Ј® D 2Ј® C 3Ј®D 4Ј®A 5Ј®B 6Ј®C 7Ј®C 8Ј®C 9Ј®C 10Ј®B 11Ј®D 12Ј®D
¶юЈ®І»¶ЁПоСЎФсМвЈЁГҝРЎМв4·ЦЈ¬№І12·ЦЎЈГҝРЎМвУРТ»ёц»тБҪёцСЎПо·ыәПМвТвЈ¬И«ІҝСЎ¶ФөДөГ4·ЦЈ¬В©СЎөГ2·ЦЈ¬ҙнСЎІ»СЎөГ0·ЦЎЈЈ©
13Ј®BC 14Ј® B 15Ј®CD
ИэЈ®МоҝХјтҙрМвЈЁ№І35·ЦЈ©
16Ј®(6·ЦЈ¬ГҝҝХ1·Ц) (1) ўЩC ўЪA ўЫD ўЬB (2) ўЩCO2 ўЪCH4
17Ј®ЈЁГҝҝХ1·Ц№І3·ЦЈ©Чг№»өДИИБҝЈ» »ҜС§Ј» УР»ъОпЈ»
18Ј®ЈЁГҝҝХ1·Ц№І7·ЦЈ©ЈЁ1Ј©јо C ЈЁ2Ј©№эВЛЈЁЧЁУРГыҙКЈ¬іцПЦҙнұрЧЦІ»өГ·ЦЈ©
ЈЁ3Ј©»оРФМҝЈЁРҙЎ°»оРФМјЎұЎўЎ°ДҫМҝЎұІ»өГ·ЦЈ©ЈЁ4Ј©ПЎСОЛбЈЁ»тЎ°СОЛбЎұЎўЎ°ВИ»ҜЗвИЬТәЎұЎўЎ°ВИ»ҜёЖИЬТәЎұЎўЎ°ВИ»ҜұөИЬТәЎұөИЈ¬РҙЎ°БтЛбЎұЎўЎ°HClЎұ ЎўЎ°HClИЬТәЎұІ»өГ·ЦЈ© ЈЁ5Ј©№ӨТө·ПЛ®ҙҰАнҙпұкәуІЕДЬЕЕ·ЕЈЁ»тЎ°»щөШДЪЙъ»оОЫЛ®І»ТӘИОТвЕЕ·ЕЎұөИҝЖС§әПАнјҙҝЙЎўРҙЎ°Е©Т©Ўў»Ҝ·КІ»ТӘАДУГЎұІ»өГ·ЦЈ©
19Ј®ЈЁГҝҝХ1·Ц№І6·ЦЈ©ЈЁ1Ј©19.00ЈЁРҙЎ°
20Ј®(8·ЦЈ¬ГҝҝХ2·Ц) ұы ТТ ПаөИ ҪөОВҪбҫ§
21Ј®ЈЁ·ҪіМКҪ2·ЦЈ¬№І5·ЦЈ©ЈЁ1Ј©ЗвЖш ТТЈҫјЧЈҫұыЈЁ»тЎ°ТТЎўјЧЎўұыЎұЈ¬Рҙ
Ў°ұыЈјјЧЈјТТЎұІ»өГ·ЦЈ©ЈЁ2·ЦЈ© ЈЁ2Ј©Ca(OH)2 +H2SO4= CaSO4 + 2H2O (ОҙЕдЖҪҝЫТ»·Ц)
ЛДЈ®КөСйМҪҫҝМвЈЁ№І24·ЦЈ©
22Ј®ЈЁ№І8·ЦЈ©ЈЁ1Ј©BЈәјҜЖшЖҝЈ¬HЈәҫЖҫ«өЖ ЈЁ2Ј©2H2O2 2H2O+O2ЎьЈ»ЈЁ2·ЦЈ© GЈ»
2H2O+O2ЎьЈ»ЈЁ2·ЦЈ© GЈ»
ЈЁ3Ј©Л®»тПёЙі
ЈЁ4Ј©ACЈЁМо¶ФТ»ёцёш1·ЦЈ¬УРҙнІ»ёш·ЦЈ¬№І2·ЦЈ©
23Ј®ЈЁГҝҝХ1·ЦЈ¬№І6·ЦЈ© ЈЁ1Ј©СО ЈЁ2Ј©іОЗеКҜ»ТЛ® іОЗеКҜ»ТЛ®ұд»лЧЗ(РҙЎ°УР°ЧЙ«іБөнЙъіЙЎұЎўЎ°УРіБөнЙъіЙЎұҫщҝЙөГ·Ц) ЈЁ3Ј©ҝм Т»Ж¬СРЛйөДТ©Ж¬
ЎҫНШХ№МҪҫҝЎҝ¶ФЙнМеОЮәҰЈЁ»тЎ°°ІИ«ОЮ¶ҫЎұөИҫщҝЙөГ·ЦЈ©
24Ј®ЈЁГҝҝХ2·Ц№І10·ЦЈ©ЈЁ1Ј©ЖшГЬРФЈЁ2Ј©BЈ»ЈЁ3Ј©2Al+6HCl=2AlCl3+3H2ЎьЈ»І»ДЬЈ»ТтОӘёГ·ҙУҰ»б·ЕіцЖшМеЈ¬ОЮВЫёГ·ҙУҰКЗІ»КЗ·ЕіцИИБҝЈ¬өј№ЬҝЪ¶ј»бУРЖшЕЭГ°іцЎЈ
ОеЈ®јЖЛгМвЈЁ№І13·ЦЈ©
25Ј®ЈЁГҝҝХ2·Ц№І6·ЦЈ©
ЈЁ1Ј©27ЈЁ2Ј©72ЎГ5 ЈЁ3Ј©72
26Ј®ЈЁ№І7·ЦЈ©ЈЁ1Ј©ЈЁГҝҝХ2·ЦЈ© = Na2SO4ЈЁ2Ј©ЈЁ3·ЦЈ© 12%
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com