
题目列表(包括答案和解析)
物质A、B、C、D、E、F、G、H、I、J有如图所示的转化关系。

图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素。其它信息见下表:
|
编号 |
信 息 |
|
1 |
D为地壳中含量最高的元素组成的单质 |
|
2 |
E为酸性气态氧化物 |
|
3 |
F的浓溶液常做干燥剂 |
|
4 |
H为淡黄色固体化合物 |
|
5 |
电解饱和J溶液是工业重要反应 |
|
6 |
C为离子化合物,阴、阳离子均含有金属元素 |
(1)写出G的化学式: ,指出H中化学键的类型: 。
(2)常温下测得一定浓度的C溶液的pH=10,用离子方程式表示其原因 。
(3)写出与H相对分子质量相同,且它们的阴离子所含的电子数、电荷数也均相同的化合物的化学式 。
(4)写出C溶液中通入过量CO2的化学方程式: 。

(5)通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中三种含Y元素的离子,其中两种离子物质的量(n)与反应时间(t)的变化示意图如上图所示,写出该反应的离子方程式是 ,该苛性钾溶液中KOH的质量是 g。
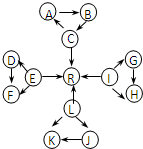 元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):
元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):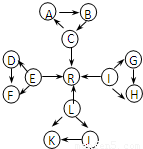
某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应物或生成物已略去)。已知①图中每个小三角形的三种物质中至少含有一种相同元素,K与L、A与B分别含有相同的元素。②D,J为固体单质,R为气体单质,其余为常见化合物。③A能使品红溶液褪色,也能使澄清石灰水变浑浊。④E为淡黄色化合物,E与C或L反应都能生成R。⑤I为氧化物,I与F或C都能反应;G和L反应生成难溶物H,H具有较强的吸附性。
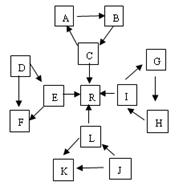
(1) J物质的化学式为 ,B所形成的晶体
为 晶体,工业上要让B转化为C,与B反应的原料是 。
(2)标况下,由E生成R 11.2 L时转移的电子数为 。
(3)C+J![]() A+L的化学方程式为: 。
A+L的化学方程式为: 。
I+F→G的离子方程式为: 。
(4)常温下,测得一定浓度的G溶液的pH=10,试用离子方程式表示其原因 。
(5)J的最简单氢化物可与空气在碱性溶液中形成燃料电池,其负极电极反应式为 。

 A+L的化学方程式为: 。
A+L的化学方程式为: 。 。
。 。
。1D
19.(1)
MnO2 + 4HCl(浓)
 MnCl2
+ Cl2↑+ 2H2O(2分)
MnCl2
+ Cl2↑+ 2H2O(2分)
(2) 检查装置的气密性(1分)
C:出现淡黄色沉淀(出现浑浊)(1分)D:浅绿色溶液变成黄色;(1分)
E:淀粉溶液变蓝(1分) F:出现白色沉淀(1分)
(3) 2Fe2++ 4Br-+ 3Cl2 = 2Fe3++ 2Br2 + 6Cl-(2分)
(4) 强碱溶液 (1分) 2OH -+ Cl2 = Cl- + ClO- + H2O(2分)
(5) B中液面下降,液面上方充满黄绿色气体,长颈漏斗中液面上升;(2分)
收集尾气,防止污染大气(2分)
20.肯定含有CO32-、SO42-、 Cl-,可能含有NO3-(每个一分共4分)
21.(1)Fe;Cl2;H2;(2)(2分)4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)(2分)2Fe2++Cl2=2Fe3++2Cl-(每个2分共10分)
 22.(1) ①Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
22.(1) ①Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
或Na2SO3+H2SO4=Na2SO4+SO2↑+2H2O
②2Na2O2+2CO2=2Na2CO3+O2↑
(2) ①2Na2O2+2H2O=4Na++4OH-+O2↑
②Al2O3+2OH-=2AlO- 2+H2O
(3) AlO- 2+2H2O Al(OH)3+OH- (每个2分共10分)
Al(OH)3+OH- (每个2分共10分)
23. ⑴Na2CO3+HCl=NaCl+Na2CO3
⑵HCO3-+H+=H2O+CO2
⑶
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com