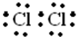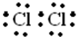(2009?朝阳区一模)已知反应 ①、②是化工生产中的两个重要反应:
①甲溶液
A+B+C
②乙经过粉碎后在沸腾炉中燃烧,得到D和E
其中,A、D在常温常压下为刺激性气味气体,C为无色无味气体.请回答:
(1)A的电子式是
.
(2)将A通入B的溶液中,反应的离子方程式是
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.
(3)1g C在A中燃烧时放出92.3kJ的热量,该反应的热化学方程式是
H2 (g)+Cl2(g)=2HCl (g);△H=-184.6kJ/mol
H2 (g)+Cl2(g)=2HCl (g);△H=-184.6kJ/mol
.
(4)工业上可利用E为原料冶炼其中所含的金属,方法是
热还原法
热还原法
.
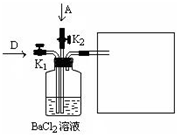
(5)将A和D按物质的量1:1通入如图装置中:
该过程中的化学方程式是
Cl2 +SO2+BaCl2+2H2O=BaSO4↓+4HCl
Cl2 +SO2+BaCl2+2H2O=BaSO4↓+4HCl
.
上述实验装置设计不完整,请将所缺部分在装置图的右边方框中画出.
(6)一定条件下,将12g乙放入过量的浓硝酸中,反应过程中转移1.5mol电子,该反应的离子方程式是
FeS2 +14H++15NO3-=Fe3++2SO42-+15 NO2↑+7H2O
FeS2 +14H++15NO3-=Fe3++2SO42-+15 NO2↑+7H2O
.