
题目列表(包括答案和解析)
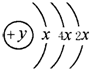 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空: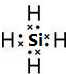
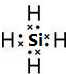
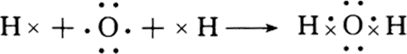
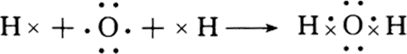


| ||
| ||
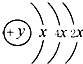 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.D 2.C 3.D 4.C 5.C 6.C 7.D 8.B 9.B 10. B
二、选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。若正确答案只有一个选项,错选、多选均不得分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得3分,但只要选错一个,该小题为0分。)
11.A 12.BD 13.BD 14.B 15.BD 16.AC 17.CD 18.B
三、(本题包括两小题,共20分)
19.(10分)(1) (2分)
O
Mg
Al
S
Cl
(2)  (2分)
(2分)
(3)Mg>Al>S>Cl>O (2分)
(4)HClO4 (2分)
(5)离子键(2分)
20.(10分)OH-,NH4+,H2O,NH3,H3O+ (各2分)
四、(本题包括两小题,共22分)
21.(10分).(1)硅,SiH4
(2)N<P<Si<Mg
(3)Mg(OH)2 HNO3 (每空2分)
22.(12分)(1)Cl2、KCl(或KClO)、KClO(KCl)、KClO3;
(2)Cl2+2KOH=KCl+KClO+H2O;
2KClO3 △ 2KCl+3O2↑ (每空2分)
五、(本题包括两小题,共14分)
23.(6分)(1)24 (3分)
(2)23mol (3分)
24.(8分)因B原子的L层电子数是K层的3倍可知B为氧原子,这样0.8gBY
 M(A)
M(A)
=
即A为P。(2分)
因为当原子个数相等时,分子个数比为3∶4 则P和O的单质为P4和O3 (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com