
题目列表(包括答案和解析)
| ||
| ||
| ||
| ||
 2H2↑+O2↑
2H2↑+O2↑ 2Fe+3CO2
2Fe+3CO2 Cu(NO3)2+2NO2↑+2H2O
Cu(NO3)2+2NO2↑+2H2O 6Cu+SO2↑,该反应中氧化产物与还原产物的质量比______.
6Cu+SO2↑,该反应中氧化产物与还原产物的质量比______.
| ||
| ||
| ||
| ||
 2H2↑+O2↑
2H2↑+O2↑ 2Fe+3CO2
2Fe+3CO2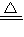 Cu(NO3)2+2NO2↑+2H2O
Cu(NO3)2+2NO2↑+2H2O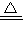 6Cu+SO2↑,该反应中氧化产物与还原产物的质量比______.
6Cu+SO2↑,该反应中氧化产物与还原产物的质量比______.(14分)在化学反应中,只要物质所含元素的化合价发生变化的反应就是氧化还原反应。例如:2Na+C12 =2NaCl,反应前后,Na元素、Cl元素的化合价分别发生了变化,该反应是氧化还原反应。
(1)根据化合价是否变化分析,下列反应(部分反应条件略去)属于氧化还原反应的是
(填写序号);
①C+O2 == CO2 ②CaO+H2O==Ca(OH)2 ③CaCO3==CaO+CO2↑
④2H2O2 == 2H2O+O2↑ ⑤CO+CuO=Cu+CO2 ⑥HCl+NaOH=NaCl+H2O
(2) 含有高价态元素的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁。试回答下列问题:
①该反应的化学方程式可表示为 ;
②向上述反应后的溶液中加入过量的锌粉充分反应后过滤,则滤纸上一定有的固体是
(写化学式,下同),滤液中的溶质是 。
(3) 通过进一步定量分析上述氧化还原反应的化合价变化发现:氧化还原反应中其元素化合价升高总数 (填“大于”、“等于”或“小于”)化合价降低升高总数。氟气是氧化性最强的非金属单质,在加热条件下,等物质的量的F2和烧碱完全反应,生成NaF、H2O和另一种气体,该气体可能是_______。 (写化学式)
(4)柠檬果汁中含有维生素C(C6H8O6,简写成Vc)是还原剂,它能被I2氧化生成C6H6O6。当前市场上测定柠檬果汁中Vc含量的方法是取10.00mL果汁,用醋酸酸化,再加入20.00mL 0.02500 mol?dm-3标准碘溶液,然后以淀粉溶液作指示剂,最后用0.01000 mol?dm-3Na2S2O3标准溶液滴定过量的I2,消耗Na2S2O3溶液10.00mL。
①Vc中碳元素的平均化合价是 。
②写出Vc与I2反应的离子方程式。
③此份果汁中含Vc= mg/100mL果汁。
1-5AAAAC 6-10BBC AD AD 11-15CB AD CD 16-20 ABABCA 21-25 ACCBA 26-28CCD
29.8分
(1) 碳(或C) (2分)
(2) 
(3) 35.5
30、(12分)(1)(2分)N≡N; 三角锥(错字不给分)
(2)(6分)  略; H2O2+SO2=H2SO4; 4OH――4e―=O2+
2H2O
略; H2O2+SO2=H2SO4; 4OH――4e―=O2+
2H2O
(3)(2分)水迅速冲入试管的,收集的是氨气;水面缓慢上升的,收集的是SO2;
(4)(2分)c(OH―)< c(NH4+)< c(SO42―)< c(H+)
31、14分(1)Na2SO3、NaOH、Na2SO4(2分)
(2)必须在密闭系统中(或在通风厨中)进行,防止污染空气(或防止中毒)(1分);黑色沉淀中有还原性物质,浓硝酸的氧化性强于浓硫酸。(2分)
(3)硫(或S)(1分),硫微溶于酒精但不溶于水,将硫的酒精溶液倒入水中,即可析出固体硫(1分)
(4)Cu2O+4NH3?H2O=2[Cu(NH3)、2]++2OH―+3H2O(2分)
4[Cu(NH3)2]++8NH3?H2O+O2=4[Cu(NH3)4]2++4OH―+6H2O(2分)
|