
题目列表(包括答案和解析)
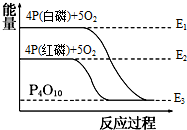 (2013?浦东新区一模)白磷和红磷与氧气反应过程与能量的变化关系如图,E表示能量,则下列说法正确的是( )
(2013?浦东新区一模)白磷和红磷与氧气反应过程与能量的变化关系如图,E表示能量,则下列说法正确的是( )| 5 |
| 4 |
| 1 |
| 4 |
| 5 |
| 4 |
| 1 |
| 4 |
在25℃101 kPa下,白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程
式分别为:P4(s)+5O2(g)= P4O10(s);△H = -3093.2 kJ/mol
4P(s)+5O2(g)= P4O10(s);△H = -2954.0 kJ/mol
由此判断,下列说法正确的是 ( )
(A)由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
(B)由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
(C)由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
(D)由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
1―18 BCDAA BDADB DBBCC BDB
19.(1)略(3分)
(2)根据转移电子分析:4 x 2.5 x 2=n(BrF3) x 3 n(BrF3)=16/15 mol(3分)
20.略
21.略
22.(1)abc
(2)c
|