
题目列表(包括答案和解析)
甲、乙、丙三个实验小组分别进行测定Na2CO3和NaOH混合物中Na2CO3含量的实验。
(1)甲组:沉淀分析法
把m g混合物溶解后假如过量BaCl2,然后将所得沉淀过滤、洗涤、烘干、称量,固体质量为w g,根据沉淀质量计算原混合物中Na2CO3质量分数为 。写出反应的离子方程式 。如果原溶液中过量的Ba2+浓度达到0.01mol/L,则溶液中残留的CO32-的质量的量浓度是 。(Ksp(BaCO3)=2.58×10-9)
(2)乙组:气体分析法

把m g混合物与过量盐酸反应后,用如上图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是 ,选用该溶液后实验结果还是不准确,原因是 。针对上述问题,乙组同学改用测定反应结束后容器A中溶质质量的方法测定Na2CO3和NaOH混合物中Na2CO3含量,如果在加热蒸发的过程中操作不当引起固体飞溅,则测出的样品中Na2CO3的质量分数将 。(填“偏大”或“偏小”)
(3)丙组:滴定分析法
称量m g混合物试样于锥形瓶中,加水使之溶解后,加酚酞指示液2滴,用c mol/LHCl标准滴定溶液至溶液由红色恰好变为无色(Na2CO3+HCl===NaHCO3+NaCl),消耗HCl 溶液V1mL,然后,加入甲基橙指示液1~2滴,继续用HCl标准滴定溶液滴定至溶液由黄色变为橙色(NaHCO3+HCl==NaCl+CO2↑+H2O),消耗HCl溶液V2mL。则样品中Na2CO3的质量分数为 。

(1)甲组:中和滴定法
滴定时用到的主要试剂是:标准盐酸和_____________________________,用到的2件主要玻璃仪器是_______________________________。
(2)乙组:气体分析法
称取一定量的混合物与足量盐酸反应,用上图装置测定产生的CO2气体的体积,为减小CO2在B中溶液的溶解质量,B中应盛放_____________溶液,选用该溶液后实验结果可能不够精确,主要原因是________________________________________________________________
____________________________________________________________________。
(3)丙组:沉淀分析法
称取一定量的混合物溶解后加入过量CaCl2溶液,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是_________________________________________________
____________________________________________________________________。洗涤沉淀多次,检验沉淀是否洗净的操作是_________________________________________。
 某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动:
某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动: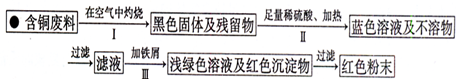

(1)甲小组进行中和滴定实验,实验室里提供了下面几种仪器:酸式滴定管、碱式滴定管、量筒、托盘天平、普通漏斗、玻璃棒、烧杯,你认为还缺少的玻璃仪器是__________。
(2)乙小组设计了如下图所示的一套实验装置,以探究该装置的多功能性。

①李明同学认为该装置可以用来制取、收集SO2气体,其中Ⅲ中盛有NaOH溶液。乙小组同学经过讨论后认为该装置存在安全隐患,需要将Ⅲ进行改装,请将改装后的装置图画在方框内。
②王强同学认为可利用该装置快速制取、净化、收集氨气。其中Ⅱ中盛有浓硫酸。你认为是否正确,若正确则不需作答;若不正确,提出改进意见___________________。
(3)丙小组进入了一家回收含铜电缆废料的工厂做社会调查,技术员向同学们展示了两个处理方案,并向同学们提出下列问题:
方案1:

方案2:

①你认为方案___________________更符合当前绿色生产的理念。
②写出方案1中步骤Ⅱ反应的离子方程式__________________。
③技术员指出,无论是方案1还是方案2,都应加入稍过量的铁屑并最终除去,请你设计出去铁屑的操作方法______________________________________________________。
④为了增加经济效益,该工厂把最后一步所得浅绿色溶液,通过__________________、冷却结晶、过滤、洗涤、自然干燥得到一种俗称“绿矾”的工业产品。
⑤丙组同学经查询资料、研究、讨论,又设计了方案3,即把方案2中“加入足量稀硫酸、通入空气并加热”改为“加入足量稀硫酸和H2O
 某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动:
某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动: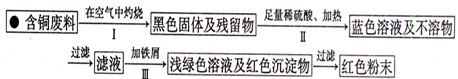

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com