
题目列表(包括答案和解析)
| A、纯碱(NaOH) | B、甲醛(CH3OH) | C、石膏(CaSO4?2H2O) | D、生石灰[Ca(OH)2] |
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |

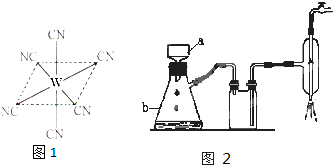
请回答:
(1)a试剂最好选用:________,其作用是:
①________;②________;③________。
(2)b试剂最好选用下列________。
①盐酸 ②氢氧化钠溶液 ③硫酸
(3)分离操作方法Ⅱ的名称是________,该操作通常用于________的分离。
(4)某同学设计如下实验:在未用指示剂的情况下,向原混合物中加入足量NaOH溶液,然后进行蒸馏,结果蒸馏出来的物质中几乎没有乙酸乙酯。请说明原因,并写出有关反应的化学方程式。
乙酸乙酯中混有乙酸和乙醇,下图是对该混合物进行分离操作步骤流程图。(括号内为所用试剂,方括号内为分离操作方法)
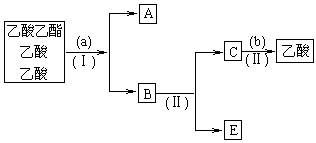
请回答:
(1)a试剂最好选用:________,其作用是:
①________;②________;③________。
(2)b试剂最好选用下列________。
①盐酸 ②氢氧化钠溶液 ③硫酸
(3)分离操作方法Ⅱ的名称是________,该操作通常用于________的分离。
(4)某同学设计如下实验:在未用指示剂的情况下,向原混合物中加入足量NaOH溶液,然后进行蒸馏,结果蒸馏出来的物质中几乎没有乙酸乙酯。请说明原因,并写出有关反应的化学方程式。
一、选择题
CDCCD
|