
题目列表(包括答案和解析)
I.实验室有一瓶失去标签的某白色固体,已知其成份可能是碳酸或亚硫酸的钠盐或钾盐,
且其成分单一。现某化学小组通过如下步骤来确定其成分:
⑴阳离子的确定:
实验方法及现象: 。
结论:此白色固体是钠盐。
⑵阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
II.确认其成分后,由于某些原因,此白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤I 称取样品1.000 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1 KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
⑴写出步骤III所发生反应的离子方程式 。
⑵在配制0.01 mol·L-1 KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量 (填“偏大”、“偏小”或“无影响”)
⑶滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
则该变质固体中X的质量分数为 。
I.实验室有一瓶失去标签的某白色固体,已知其成份可能是碳酸或亚硫酸的钠盐或钾盐,
且其成分单一。现某化学小组通过如下步骤来确定其成分:
⑴阳离子的确定:
实验方法及现象: 。
结论:此白色固体是钠盐。
⑵阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
II.确认其成分后,由于某些原因,此白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤I 称取样品1.000 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1 KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
⑴写出步骤III所发生反应的离子方程式 。
⑵在配制0.01 mol·L-1 KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量 (填“偏大”、“偏小”或“无影响”)
⑶滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
则该变质固体中X的质量分数为 。

| ||
| ||
| ||
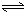 H2SiO3+2OH-(或SiO32-+H2O
H2SiO3+2OH-(或SiO32-+H2O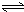 HSiO3-+OH-,HSiO3-+H2O
HSiO3-+OH-,HSiO3-+H2O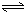 H2SiO3+OH-,AlO2-+H2O
H2SiO3+OH-,AlO2-+H2O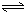 Al(OH)3+OH-),降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全
Al(OH)3+OH-),降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全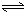 H2SiO3+2OH-(或SiO32-+H2O
H2SiO3+2OH-(或SiO32-+H2O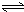 HSiO3-+OH-,HSiO3-+H2O
HSiO3-+OH-,HSiO3-+H2O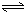 H2SiO3+OH-,AlO2-+H2O
H2SiO3+OH-,AlO2-+H2O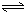 Al(OH)3+OH-),降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全
Al(OH)3+OH-),降低pH值有利于平衡向正反应方向移动,当pH调到7~8时,使它们水解完全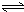 Cr2O72-+H2O
Cr2O72-+H2O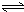 Cr2O72-+H2O
Cr2O72-+H2O某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:一是发生氧化还原反应;二是发生双水解反应:2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3。为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
(1)、 写出发生氧化还原反应的离子方程式 ;
(2)实验Ⅰ,学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,设计这个实验的目的是___________________。
(3)实验Ⅱ,取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色液体是___________________。向红褐色液体中逐滴加入稀盐酸至过量。将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,反应的离子方程式为__________________。另一份加入BaCl2稀溶液,有少量白色沉淀生成。
(4)实验Ⅲ,换用稀释的FeCl3和Na2SO3溶液重复实验Ⅱ、Ⅲ,产生的现象完全相同。由上述实验得出的结论是______________________________________。若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是___________________________________________。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①________________________________________________________________;
②________________________________________________________________。
Ⅱ.(5分)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓氢氧化钠溶液。将发生一系列变化。已知,NH4+与AlO2- 在水溶液中不能大量共存,会发生如下反应: NH4++A102-+H2O=Al(0H)3↓+ NH3↑
试回答:
(1)硫酸铝铵在水溶液中的电离方程式为 ;
(2)在逐滴加入浓氢氧化钠溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气体逸出;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀逐渐减少。请回答各种现象由先到后出现的顺序是(用序号回答): ;
(3)写出滴入氢氧化钠溶液的过程中,有关反应的离子方程式:
① ;
② ;
③ ;
1.B 2.B 3.D 4.D 5.C
30.(每空2分,共20分)
(1)增多 条件反射 (2)④ (3)突起(树突)(不能答轴突)
(4)高尔基体 细胞质 组织液 A (5)下丘脑 持续性兴奋或抑制
 31.I(12分)
31.I(12分)
 ⑴①
⑴①
② (每空1分)
⑵温度 15 (3分) ⑶右(或右上)(1分)
⑷无光(或黑暗)(2分) ⑸(参见下图①、②各2分)



II.(10分)
(1)由于重力作用,幼苗茎近地侧生长素 分布
比远地侧多,近地侧生长快(2分)
(2)装置A置于光下,光干扰了生长素较快地
移至近地侧(或光引起生长素分解)(2分)
(3)装置图3分(花盆侧放1分、单侧光从下
方进入2分)
预测并分析实验结果:(各1分)
①幼苗水平生长,重力与单侧光照射对幼苗生长影响相同
②幼苗向上弯曲生长,重力对幼苗生长影响比单侧光对幼苗生长的影响强
③幼苗向下弯曲生长,重力对幼苗生长影响比单侧光对幼苗生长的影响弱
化学答案
6.A 7.D 8.C 9.A 10.C 11.B 12.D 13.B
26.(14分)
(1)红褐 (1分)
4Fe(OH)2+O2+2H2O=4Fe(OH)3 (2分)
(2)2H2S+SO2=3S+2H2O (2分)。
 NaOH(或碱液)
(2分)
NaOH(或碱液)
(2分)
(3)NO(1分);
3NO2+H2O=2HNO3+NO(2分)。
(4)(黄绿色变为)无色(1分); 5(3分)。
27.(16分)
(1)关闭活塞A,向左侧漏斗加水,若漏斗下端能形成水柱,静止一段时间,水柱的高度不再发生变化,证明装置的气密性良好。(2分)
(2)b (2分)
(3)U形管中出现蓝色沉淀 (2分)
2Na+2H2O=2Na++2OH-+H2↑ Cu2++2OH-=Cu(OH)2↓
或 2Na+2H2O +Cu2+=2Na++Cu(OH)2↓+H2↑ (3分)
(4)检验氢气纯度。(2分)
(5)M=m/( m―3.796) (3分)
(6)待装置内气体的温度恢复至室温后,调节A管使左右液面持平。(2分)
28.(16分)
(1) 四 Ⅷ (2分)
(2)⑦ (2分)
(3) 3Fe+4H2O(g) Fe3O4+4H2 (3分)
Fe3O4+4H2 (3分)
(4)加少量KClO3,插上镁条并将其点燃 (2分)
焊接钢轨(制高熔点金属)(其他合理答案也给分)(2分)
(5)2Al+2OH-+2H2O=2AlO2-+3H2↑ (3分)
(6)Al3++3e-=Al (2分)
29.(14分)
(1)C9H8O4 (2分) (2)AC (2分)
(3)4 (2分) 取代反应、加成反应(2分)
 (4)(每空3分)
(4)(每空3分)

 |
物理参考答案
题号
14
15
16
17
18
19
20
21
答案
D
A
BC
AC
C
D
BD
BD
22.(17分)
|