
题目列表(包括答案和解析)
I.恒温、恒压下,在一个可变容积K*s^5#u的容器中发生如下发应:A(气)+B(气)![]() C(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时AK*s^5#u的物质K*s^5#u的量
为 mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成CK*s^5#u的物质K*s^5#u的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和CK*s^5#u的物质K*s^5#u的量分别是ymol和3a mol,则x= mol,y= mol。平衡时,BK*s^5#u的物质K*s^5#u的量
(甲) >2 mol (乙)=2 mol (丙)< 2 mol (丁)可能大于、等于或小于2mol
(4)若在(3)K*s^5#u的平衡混合物中再加入3molC,待再次到达平衡后,CK*s^5#u的物质K*s^5#u的量分数是 。
(5)若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定K*s^5#u的容器中发生上述反应。开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中K*s^5#u的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和bK*s^5#u的大小
(6) A(气)+B(气)![]() C(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新K*s^5#u的平衡时,BK*s^5#u的浓度是原来K*s^5#u的60%,则
C(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新K*s^5#u的平衡时,BK*s^5#u的浓度是原来K*s^5#u的60%,则
A.平衡向正反应方向移动了 B.物质AK*s^5#u的转化率增大了
C.物质BK*s^5#u的质量分数增加了 ![]() 混合气体K*s^5#u的平均相对分子质量减少了
混合气体K*s^5#u的平均相对分子质量减少了
II. 某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
一级电离:H2A![]() H++HA- 二级电离:HA-
H++HA- 二级电离:HA-![]() H++A2-
H++A2-
已知相同浓度时K*s^5#u的电离度a(H2A)>d(HA-),设有下列四种溶液:
A.0.01mol.L-1K*s^5#u的H2A溶液 B.0.01mol.L-1K*s^5#u的NaHA溶液
C.0.01mol.L-1K*s^5#u的HCl与0.04mol.L-1K*s^5#u的NaHA溶液等体积混合液
D.0.02mol.L-1K*s^5#u的NaOH与0.02 mol.L-1K*s^5#u的NaHA溶液等体积混合液
![]()
![]() 据此,填写下列空白(填代号)
据此,填写下列空白(填代号)
(1) c(H+)最大K*s^5#u的是__________,最小K*s^5#u的是__________。
(2) c(H2A)最大K*s^5#u的是_________,最小K*s^5#u的是__________
(3) c(A2-)最大K*s^5#u的是___________, 最小K*s^5#u的是________。
 乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.
乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.| M2+ | K[(MY)2-] | Ksp(MS) | 填“是”或“否” |
| Pb2+ | 2×1018 | 4×10-26 | |
| Cd2+ | 2.6×1016 | 1×10-20 |
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
| 0.01-x |
| x×(0.49+x) |
| 0.01 |
| 0.49x |
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
| 0.01-x |
| x×(0.49+x) |
| 0.01 |
| 0.49x |
| ||
| ||
| 催化剂 |
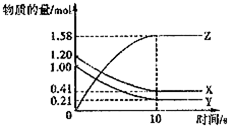 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com