
题目列表(包括答案和解析)
(12分)某研究性学习小组的课题为“Mg—Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如下图所示(C1、C2均为碳棒),按要求填写下列空格。
(1)铜片上的现象是 ,该极的电极反应式为 。
(2)C1极的名称为 ,C2极的电极反应式为 。
(3)下列关于该装置中电子流向的叙述中正确的是 。
| A.从镁电极经导线流向C1极 | B.从C1极经导线流向镁电极 |
| C.从铜电极经导线流向C2极 | D.从C2极经导线流向铜电极 |
(12分)某研究性学习小组的课题为“Mg—Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如下图所示(C1、C2均为碳棒),按要求填写下列空格。
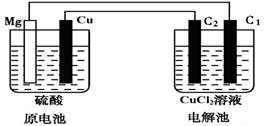
(1)铜片上的现象是 ,该极的电极反应式为 。
(2)C1极的名称为 ,C2极的电极反应式为 。
(3)下列关于该装置中电子 流向的叙述中正确的是 。
A.从镁电极经导线流向C1极 B.从C1极经导线流向镁电极
C.从铜电极经导线流向C2极 D.从C2极经导线流向铜电极
(4)原电池中稀硫酸的体积为200 mL ,物质的量浓度为1.5 mol·L-1,当电解池中某碳棒上产生3.36 L(标准状况)气体时,求:
① 有 个电子通过了电线(NA=6.02×1023) 。
② 此时原电池溶液中H+的物质的量浓度为 mol/L (不考虑溶液体积变化)。
某研究性学习小组的课题为“Mg—Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如下图所示(C1、C2均为碳棒),按要求填写下列空格。
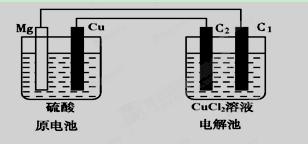
(1)铜片上的现象是 ,该极的电极反应式为 。
(2)C1极的名称为 ,C2极的电极反应式为 。
(3)下列关于该装置中电子 流向的叙述中正确的是 。
A.从镁电极经导线流向C1极 B.从C1极经导线流向镁电极
C.从铜电极经导线流向C2极 D.从C2极经导线流向铜电极
(4)原电池中稀硫酸的体积为200 mL ,物质的量浓度为1.5 mol·L-1,当电解池中某碳棒上产生3.36 L(标准状况)气体时,求:
① 有 个电子通过了电线(NA=6.02×1023) 。
② 此时原电池溶液中H+的物质的量浓度为 mol/L (不考虑溶液体积变化)。
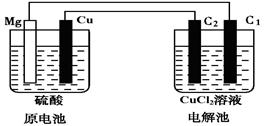
| A.从镁电极经导线流向C1极 | B.从C1极经导线流向镁电极 |
| C.从铜电极经导线流向C2极 | D.从C2极经导线流向铜电极 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com