
题目列表(包括答案和解析)
中学化学中有一类物质其氧化性强弱与物质的浓度有关,溶液的浓度不同时反应产物不相同。下列各组物质中具备上述性质的是 ( )
①Cu与HNO3溶液 ②Cu与FeC13溶液
③Zn与H2SO4溶液 ④Fe与HC1溶液
A.①② B.②③ C.③④ D.①③
|
中学化学中有一类物质其氧化性强弱与物质的浓度有关,溶液的浓度不同时反应产物不相同.下列各组物质中具备上述性质的是 ①Cu与HNO3溶液 ②Cu与FeC13溶液 ③Zn与H2SO4溶液 ④Fe与HC1溶液 | |
A. |
①② |
B. |
②③ |
C. |
③④ |
D. |
①③ |
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
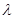 与光的频率v的关系为
与光的频率v的关系为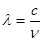 ,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因:
,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因: | 共价键 | C—C | C—N | C—S |
| 键能/kJ·mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(1)提出假设:A是FeCl3,B是FeCl2。
(2)设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同。请填写下表中的相应空格。
实验方法 | 实验现象 | 结论 |
分别向A、B溶液中加KSCN溶液 | ________ | 固体物质中有FeCl3 |
分别向KMnO4溶液中加适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含_______ |
(3)根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式:___________________。
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是____________________________________________________________________。
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)实际应用:
FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeCl3、FeCl2、CuCl2,某研究性学习小组的同学们设计了两种从废液中回收Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为:_______________。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的Cu已全部析出。方案2中铜作 极,所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)_____________。
方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:________________。
类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成 Fe ( NO3)3,但当铁过量时,产物是 Fe (NO3) 2 。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当 C12 足量时生成 FeC13 , 当铁粉过量时产物是 FeCl2 。为验证该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的 C12 中点燃,取其表面生成物并分别编号为 A、B ,然后通过实验确定其成分。
探究过程如下:
提出假设: A 是 FeCl3 , B 是 FeCl2 。
(1) 设计实验方案:分别取 A、B 的溶液均进行以下实验,但实验现象相同。请填写下表中的相应空格。
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | ____________________ | 固体物质中有FeCl3 |
| 分别向KMnO4溶液中加适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含_______ |
(2)根据上述实验结论,写出C12与铁粉加热时发生反应的化学方程式:
____________________________________________________________。
(3)为进一步探究 FeC13 溶液的性质,他又利用 A 溶液做了如下一些实验,其中明显错误的是_______________(填写序号)。
A.将 A 溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向 A 溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在 A 溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将 A 溶液加热蒸干并灼烧,得到FeC13固体
(4)FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有 FeC13、FeCl2、CuCl2,
某研究性学习小组的同学们设计了两种从废液中回收 Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜。
该方案中涉及的四种阳离子的氧化性由强到弱的顺序为:
方案2 :在废液中加入适量的盐酸调节溶液的 pH = 1 ,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的 Cu 已全部析出。该方案中铜作_________极,该电极上所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)______________________________________________________________。
方案2 在电极上直接回收铜,操作上比方案 1 简便,但方案 2 也有不足之处,主要表现为:____________________________________
1.D 2.C 3.D 4.C 5.A 6.D 7.C 8.D 9.C
10.D 11.D 12.D 13.C 14.B 15.A
16.(1)Fe2(SO4)3(1分)
(2)SnC12; SnC14(各1分)
得2×e -
 |
 |
||

 (3)Fe2(SO4)3+SnC12+2HC1==2FeSO4+SnC14+H2SO4(2分)
(3)Fe2(SO4)3+SnC12+2HC1==2FeSO4+SnC14+H2SO4(2分)
 |
失2e -
(4)1:2(2分)
17.(1)第三周期VIA族(1分)
(2)CO2属于分子晶体而SiO2属于原子晶体(2分)
(3)NH3+HNO3 NH4NO3(2分)
(4)H2S、SiH4、C2H2H4(写出3种即可)(3分)
△
18.(1)MnO3+4H-+2C1- Mn2-+C12↑+2H2O(2分)
(2)III(1分)
(3)H+; HC1O; C12 (各1分)
(4)溶液由无色变成蓝色(1分)
(5)通过分液漏斗注入一定量的NaOH溶液,再摇动烧瓶使之充分反应(2分)
19.(1)NaHCO3; Na2CO3(各1分)
(2)C1O‑+CO2+H2O HCO3-+HC1O(2分)
(3)2(2分)
(4)C12+Na2CO3+H2O NaC1+NaHCO3+HC1O(2分)
20.(1)不能确定:Ba2+、Mg2_
(2)
阴离子符号
物质的量浓度(mol?L―1)
SO42-
0.1
CO32-
0.2
(3)存在:溶液中肯定存在离子是NH4+、CO32-和SO42-。经计算,NH4+的物质量为0.05mol,CO32-、SO42-的物质的量分别为0.02mol和0.01mol,根据电荷守恒,得K+一定存在(每空1分)
21.(1)小于(1分)
(2)
序号

反应①的
△H/(kJ?mol-1)
反应②的
△H/(kJ?mol-1)
总反应的
△H/(kJ?mol-1)
I
+216
+198
Ⅱ
0.5
+108
(各1分)
(3)1:15(2分)
22.(1)烧杯、胶头滴管(2分)
(2)3.95(2分)
(3)根据题意有:
Ba2+ ~ BaCrO4 ~  Cr2O72- ~
Cr2O72- ~  I2
~ 3S2O32-
I2
~ 3S2O32-
1 mol 3mol
c(Ba2+)×50.00mL×10-3L?mL-1 0.1mol?L-1×36.00mL×10-3L?mL-1
c(Ba2+)
=0.24mol?L-1(4分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com