
题目列表(包括答案和解析)
| ①提出设想 | BaCl2与NaOH不反应,与Na2CO3会生成白色沉淀. |
| ②选用仪器 | 试管(或小烧杯)、胶头滴管 |
| ③进行实验 | 用试管(或烧杯)分别取少量样品溶液,再 用胶头滴管吸取少量BaCl2溶液滴入样品溶液中 . |
| ④反应现象和结论 | 如果溶液中出现白色沉淀,则样品中存在Na2CO3,NaOH溶液已变质;如果溶液中无白色沉淀出现,则 样品中不存在Na2CO3 ,溶液未变质. |
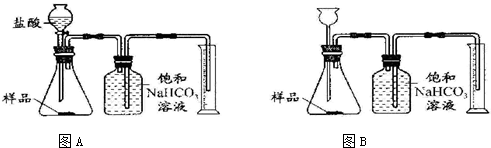
| ①提出设想 | 酸与NaOH反应 无气泡 ,与Na2CO3有气泡放出 . |
| ②选用仪器 | 试管(或小烧杯)、胶头滴管 |
| ③进行实验 | 用试管(或烧杯)取少量盐酸,再用胶头滴管吸取少量样品溶液滴入试管(或烧杯中) |
| ④反应现象 和结论 |
如果 有气泡放出 ,则样品中有Na2CO3,NaOH溶液已变质;如果 无气泡放出 ,则样品中无Na2CO3,NaOH溶液未变质. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com