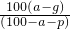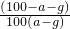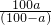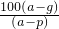(2010?聊城一模)为探究Cl
2和SO
2同时通入H
2O中发生的反应,某化学兴趣小组设计了如图所示的实验装置.
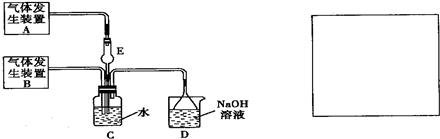
(1)化学兴趣小组的同学采用Na
2SO
3粉末与70%的硫酸反应制取SO
2气体,采用MnO
2和浓盐酸反应制取Cl
2.已知SO
2的溶解度比Cl
2大40倍,在此实验中,E仪器的作用是
防止倒吸
防止倒吸
;发生装置B应选择以下三种装置中的
①
①
(填序号)
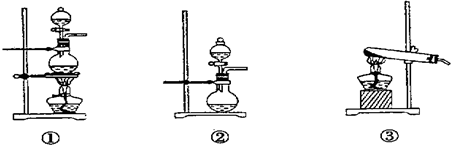
(2)资料显示等物质的量的Cl
2和SO
2同时通入H
2O中恰好反应生成两种酸,请写出反应的离子方程式
SO2+Cl2+2H2O=-4H++2Cl-+SO42-
SO2+Cl2+2H2O=-4H++2Cl-+SO42-
.
(3)为了不影响产物的检验,小组成员认为上述整套装置有一处不合理,应在
BC
BC
装置之间(填代号)连接一装置,请在装置图右边的方框中画出简易装置图,并注明装置中盛有的试剂.
(4)已知干燥的SO
2和Cl
2在活性炭催化剂存在下反应生成液态的SO
2Cl
2,反应的方程式为:SO
2(g)+Cl
2(g)?SO
2Cl
2(l)△H=-97.3KJ/mol;SO
2Cl
2溶于水得到的产物与上述实验结果相同.
①为了提高上述反应中Cl
2的平衡转化率,下列说法合理的是
AC
AC
(填序号)
A、缩小容器体积 B、使用催化剂 C、增加SO
2浓度 D、升高温度
②已知20℃时,AgCl的溶解度为1.5×10
-4g,Ag
2SO
4的溶解度为0.796g,则SO
2Cl
2溶于水所得溶液中逐滴加入AgNO
3稀溶液时,最先产生的沉淀是
AgCl
AgCl
.