
题目列表(包括答案和解析)
试管苗的光合作用能力较弱,需要逐步适应外界环境才能往大田移栽。研究人员进行了“改变植物组织培养条件缩短试管苗适应过程”的实验,实验在适宜温度下进行,图甲和图乙表示其中的两个实验结果。 请回答:
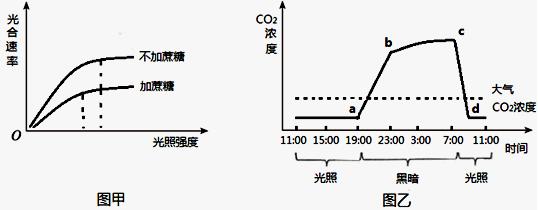
(1)图甲的实验是在大气CO2浓度下进行的。据图分析,试管苗在不加蔗糖的培养基中__________________更高。
(2)图乙是试管苗在密闭、无糖培养基条件下测得的24h内CO2浓度变化曲线。图中b-c段CO2浓度升高缓慢是因为________________________________________,c-d段CO2浓度急剧下降是因为试管苗________________________________________。若d点时打开培养瓶,试管苗的光合速率____________。
(3)根据上述实验结果推知,采用无糖培养基、____________和___________可缩短试管苗的适应过程。
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.| 10 |
| 9 |
| 10 |
| 9 |
| 1 | 2 |
| 压强 MPa 转化率/% 温度℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A、温度一定时增大压强,SO2的转化率增大 |
| B、SO2转化为SO3,最好采用600℃的温度 |
| C、用催化剂不能增大SO2的转化率,但能增加反应放出的热量 |
| D、SO2尾气可用氨水吸收 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com