
题目列表(包括答案和解析)
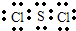
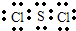
| ||
| ||
| X | Y | |
| Z | W |










(1)Y、Z、W的原子半径由小到大的顺序是______________________________。
(2)ZW2的电子式是_______________,它在常温下呈液态,形成晶体时,属于_______________晶体。
(3)工业生产单质Y的原理是______________________________ (用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是_______________。
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是_______________。
(1)Y、Z、W的原子半径由小到大的顺序是____________________。
(2)ZW2的电子式是__________,它在常温下呈液态,形成晶体时,属于__________晶体。
(3)工业生产单质Y的原理是____________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是_______________。
(5)0.1 mol的单质W与50 mL 1.5 mol·L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是____________________。
一、选择题(每小题2分,计24分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
B
D
B
C
A
A
B
C
A
B
C
B
二、选择题(每小题3分,计36分)
题号
13
14
15
16
17
18
19
20
21
22
23
24
答案
BD
A
AC
BD
D
D
AD
CD
A
D
B
AD
三、填空题
25.(本题共3分)
2H2O(l)=2H2(g)+O2(g);△H=+571.6kL/mol
26.(本题共8分)
⑴Au2O3+4Na2S2O3+2H2O=2Na2S4O6+Au2O+4NaOH
|