
题目列表(包括答案和解析)
下列说法正确的是
A.0.1mol/L的氨水和0.1mol/L的硝酸等体积混合,充分反应后所得溶液中:
c(NO3﹣)>c(NH4+)>c(OH﹣)>c(H+)
B.0.1mol/L的醋酸溶液中:c(H+)=c(CH3COO﹣)
C.将氨气通入一定量硫酸溶液中,充分反应后溶液pH=7则;c(NH4+)>c(SO42-)
D.0.1mol/L的硫化钠溶液中:c (Na+)=2c(S2-)+c(HS-)+c(H2S)
某废水处理厂处理废水中NH+的过程如下:
①NH4+
(aq)+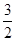 O2(g)=HNO2(aq)+H+(aq)+H2O(1)
ΔH=-b KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1)
ΔH=-b KJ/mol
②2HNO2(aq)+O2(g)=2NO3- (aq)+2H+ ΔH=-aKJ/mol
下列叙述正确的是( )
A.将NH4+转化为NO3-的热化学方程式可表示为:
NH4+ (aq)+2O2(g)=NO3-
(aq)+2H+(aq)+H2O(1) ΔH=-(b+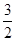 )KJ/mol
)KJ/mol
B.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
C.常温下,若HNO3溶液中c(H+)=0.1 mol·L-1,则该溶液的pH>1
D.若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)=c(NO3-)+c(H+)
在下列各溶液中,微粒的物质的量浓度关系一定正确的是
A.NaHCO3溶液中:c(OH-)+c(HCO3-)+2c(CO32-)=c(Na+)+c(H+)+2c(H2CO3)
B.氨水与 NH4Cl的混合溶液中:c(NH4+)>c(Cl-)
C.向醋酸钠溶液中加入适量醋酸得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.向硝酸钠溶液中滴加氢氧化钾溶液得到的pH=13的混合溶液:c(Na+)=c(NO3-)
下列各溶液中,微粒的物质的量浓度关系正确的是
A.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+) = c(NO3-)
B.1.0 mol·L-1Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+)
C.1.0 mol·L-1 NH4Cl溶液:c(NH4+) = c(Cl-)
D.醋酸钠溶液:c(Na+) >c(CH3COO-)>c(H+)>c(OH-)
(10分).近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
⑴有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下: ( I )将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
① 写出步骤(I)反应的化学方程式:
② 写出步骤(III)反应的离子方程式:
⑵还有学者提出利用 Fe 2十、Fe3十等离子的催化作用,常温下将SO2氧化成SO42一而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42一的转化率。

① 该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号) 。(参考:还原性SO2 > I- >Br->Cl-) 
A.碘的淀粉溶液 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.氯化钡溶液
② 若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42一的转化率,已知气体流速,还需测定的数据是 和加入盐酸酸化的氯化钡溶液后生成沉淀的质量。
(3)
为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+ Sx 、
Sx 、
CO+ Sx=COS、2COS+SO2=2CO2+
Sx=COS、2COS+SO2=2CO2+ Sx 。其中COS中“C”化合价为 。
Sx 。其中COS中“C”化合价为 。
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在消化细菌的作用下将NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇(CH3OH),NO3-和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com