
题目列表(包括答案和解析)
(1)下列实验操作或对实验事实的叙述正确的是____________(填序号)。
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.100 0 mol·L-1的KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸。
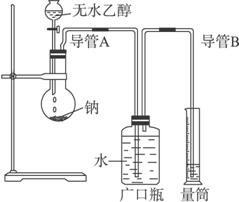
(2)为了确定乙醇分子的结构简式是CH3OCH3还是CH3CH2OH,实验室利用如上图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。
试回答下列问题:
①指出实验装置中的错误__________________________________________________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将_______________(填“偏大”“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)_____________________________________________________________________。
指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):___________________________________________。
②容量瓶:___________________________________________。
③酸式滴定管:___________________________________________。
④集气瓶(收集氯化氢):___________________________________________。
(2)下列实验操作或对实验事故的叙述正确的是_________(填序号)。
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将液溴沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融NaOH和Na2CO3固体;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸;
⑨浓H2SO4沾到皮肤上,立即用NaOH溶液清洗。
①用氨水清洗做过银镜反应的试管
②用分液漏斗分离硝基苯和水的混合物
③用湿润的pH试纸测定稀盐酸的pH
④用碱式滴定管量取20.00 mL 0.1 mol·L-1 KMnO4溶液
⑤将Na2CO3固体在瓷坩埚中加热熔融
⑥不慎将苯酚溶液沾到皮肤上,立即用NaOH稀溶液清洗
⑦向沸腾的NaOH溶液中滴加FeCl3溶液,制备Fe(OH)3胶体
⑧配制FeSO4溶液时,需加入少量的铁粉和稀硫酸
(16分)
Ⅰ.下列操作正确的是_______.
A、用氨水清洗做过银镜反应的试管
B、用酒精清洗有硫沉淀的试管
C、用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
E、如果苯酚浓溶液沾到皮肤上,应立即用70℃以上的水清洗
F、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
G、用托盘天平称取10.50 g干燥的NaCl固体;
H、向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
I、配制Al2(SO4)3溶液时,加入少量的稀硫酸。
Ⅱ.用下图装置进行SO2转化为SO3的转化率测定实验:
(1)写出圆底烧瓶中发生反应的化学方程式
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程) 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。
(4)本实验装置设计中有不恰当的地方,请指出: 。
所增加装置的目的是 。
(5)将反应生成的44.8L(标况下)SO2气体全部通过硬质玻璃管后,在右侧烧杯的试管中得到152g固体,则SO2的转化率为
【7分】请按要求填空。
下列实验操作或对实验事实的叙述正确的是_________。(填序号)
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.100 0 mol·L-1 KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸。
1-――
30.I.1)基因 没有 (2)蚕的丝蛋白基因在细菌体内得以表达
3)人类的血红蛋白是一种含Fe的特殊蛋白质
不同生物之间具有一定的亲缘关系
4)DNA→RNA→蛋白质 减轻农药对环境的污染 基因突变
II.(1)DNA 基因突变 (2)母系遗传,后代无一定的分离比
(3)害虫的天敌大量死亡 (4)不赞成。抗虫棉不是什么害虫都能抗
31 (1)Ⅰ 染色体变异和基因重组 (2)DT ddTT
(3)减数分裂第一次分裂 花药离体培养 秋水仙素
(4)1/3 2/3 (5)1┱2┱1
化学答案
选择题: 6―
26.(共14分,每空2分)(1)CuO ∶O∷C ∷O∶ 浓硫酸
(2)C+4HNO3(浓) === CO2↑+4NO2↑+2H2O (3)c
(4)2Cu2++2H2O电解====2Cu+O2↑+4H+ (5)NO
27.(共15分,最后一空3分,其余每空2分)(1)① SiO2+
2H2(g)+SiCl4(g) === Si(s)+4HCl(g);ΔH=+240.4 kJ•mol-1
② H2SiO3(或H4SiO4)和HCl 爆炸 ③ 精制的饱和食盐水 2H++2e-===H2↑
(2)4(3分)
28.( 16分)
Ⅰ①②④⑤(2分)
Ⅱ(1)无 (1分) 的反应生成Fe3+,过量的铁屑可以将Fe3+还原成Fe2+,(2分)
的反应生成Fe3+,过量的铁屑可以将Fe3+还原成Fe2+,(2分)
(2)60(2分)
(3)玻璃棒、干燥器、坩埚、泥三角(2分)连续两次加热、冷却、称量的质量差不超过
(4) (2分)
(2分)
(5)稀硫酸(2分)阳极:Fe-2e- = Fe2+ (2分)
29.(15分)
(1)

(2)①
④
⑧ (各2分)
(各2分)
⑶ ⑧,⑥,①② (各1分)
(4) 5(2分)
物理参考答案
一、选择题
14.D 15.C 16.B 17.C 18D
19.B20.B 21.D
二、实验题
22.(1)乙,偏小.(4分) (2)电流表选
23.(10分)解:(1)设撤去F时物块的速度大小为v,根据牛顿第二定律 物块的加速度 (1分),由运动学公式
(1分),由运动学公式 (1分),解得
(1分),解得 (3分)(2)设撤去F后物块还能滑行的距离为
(3分)(2)设撤去F后物块还能滑行的距离为 ,从静止到物块停下的过程中,运用动能定理
,从静止到物块停下的过程中,运用动能定理 (3分),解得
(3分),解得 (2分)
(2分)
24设杆2的运动速度为v,由于两杆运动时,两杆间和导轨构成的回路中的磁通量发生变化,产生感应电动势  ①
①
感应电流  ②
②
杆2作匀速运动,它受到的安培力等于它受到的摩擦力, ③
③
导体杆2克服摩擦力做功的功率  ④
④
解得  ⑤
⑤
解法2:以F表示拖动杆1的外力,以I表示由杆1、杆2和导轨构成的回路中的电流,达到稳定时,对杆1有  ①
①
对杆2有  ②
②
外力F的功率  ③
③
以P表示杆2克服摩擦力做功的功率,则有 ④
④
由以上各式得  ⑤
⑤
25.(20分)
 解:(1)x方向上匀速;L=v0t ① (1分)
解:(1)x方向上匀速;L=v0t ① (1分)
y方向上匀加速: ② (2分)
② (2分)
加速度: ③(2分)
③(2分)
已知 ④(1分)
④(1分)
①~④联解得; ⑤(2分)
⑤(2分)
(2)设粒子过y轴时的速度为v, 则
⑤代入⑥得, ⑦(1分)
⑦(1分)
速度方向与y轴成θ=450 ⑧(1分)
粒子在磁场中运动轨迹如图,设圆半径为r,由几何关系得:
r+rsin45°>d ⑨(2分)
 ⑩(2分)
⑩(2分)
⑦⑨⑩联解得 (2分)
(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com