
题目列表(包括答案和解析)
|
为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
| |
| [ ] | |
A. |
可用稀盐酸代替稀硫酸 |
B. |
量气管中液体为水 |
C. |
反应完全后,冷却,读取量气管体积数,再减去所加硫酸的体积,即为生成的气体体积 |
D. |
实验测得该试样中碳酸氢钠质量分数偏高,可能是测定气体体积时未冷却至室温 |
 为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是( )
为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是( )为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
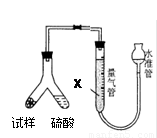
A.可用稀盐酸代替稀硫酸
B.量气管中液体为水
C.反应完全后,冷却,读取量气管体积数,再减去所加硫酸的体积,即为生成的气体体积
D.实验测得该试样中碳酸氢钠质量分数偏高,可能是测定气体体积时未冷却至室温
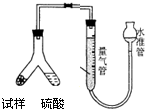 为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是为测定碳酸氢钠与碳酸铵的混合物中碳酸氢钠的质量分数,李明同学从中取出18.0g,加热,使其充分反应后,测得最终残留固体质量为5.3g。
已知(NH4)2CO3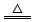 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
(1)求原混合物中碳酸氢钠的物质的量。
(2)若将实验中生成的氨气完全溶解于10 mL水中,所得溶液的密度为0.91g/cm3,求氨水的物质的量浓度(计算结果保留一位小数)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com