
题目列表(包括答案和解析)

A.0.25mol B.0.125mol C.0.100mol D.0.080mol
将Mg、Al、Zn组成的混合物与足量盐酸反应,在标准状况下产生H2的体积为2.8L,则三种金属的物质的量之和为( )
A.0.25mol B.0.125mol C.0.100mol D.0.080mol



| ||
1
2
3
4
5
6
7
8
9
10
11
12
D
A
B
C
C
D
B
B
D
D
B
D
13
14
15
16
17
18
19
20
21
22
23
C
B
A
A
D
D
A
C
C
D
D
一、选择题(每小题只有一个选项符合题意,每小题2分,共46分)
二、填空题(共54分)
24. (共9分)
(1)OH- + Al(OH)3 = AlO2- + 2H2O(2分)
(2) (1分)
(1分)
(3)Al3+
+3H2O  Al(OH)3 + 3H+ 。(2分)
Al(OH)3 + 3H+ 。(2分)
(4)SO2+Cl2+2H2O=H2SO4+ 2HCl (2分)
(5)H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H= -4QkJ/mol(2分)无负号或无聚集状态均不给分。
25、(共8分)
⑴ 10Ca(OH)2+10Cl2=2Ca(C1O)2+Ca(C1O3)2+7CaCl2+10H2O (2分)
⑵ 5 (2分)
⑶ < (2分)  (2分)
(2分)
26、(共8分)
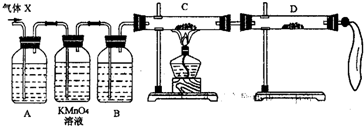
(1)X:Cl2 E: H2O2(各1分)
(2)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O(2分)无加热扣1分
Mn2++Cl2↑+2H2O(2分)无加热扣1分
Al2O3+6H+=2Al3++3H2O(2分) (3)Cl2+H2O2=2HCl+O2(2分)
27、(共9分)
(1) 减小 (1分)
(2) 1 (1分) <(1分)
(3) 正确(1分) 此反应为可逆反应,2 molX和1 molY不可能完全反应 (1分)
(4) A (2分,有错不给分)
(5)  (2分)
(2分)
28、(共10分)(1)该混合金属粉末中除镁外还含有铝(或Al)元素(1分)(2)该混合金属粉末中除镁外还含有锌(或Zn)元素(1分)(以上两空可颠倒)
(3)NaOH溶液(或氢氧化钠溶液),无“溶液”两字不扣分;(2分)
(4)在滤液中加入稀硫酸直至生成的沉淀刚好溶解,再加入足量的稀氨水(2分);
(5)步骤简单(1分),试剂节约(1分);
(6)将沉淀C洗涤、小心干燥后称量(2分)。其它合理表述均可。
 29、(共10分)
29、(共10分)
(1)醛基(错别字不得分)(1分) (1分)
|