
题目列表(包括答案和解析)
下列关于碱金属物理性质的叙述不正确的是
[ ]
A.碱金属除铯略带金色光泽外, 都呈银白色
B.碱金属都软, 有延性, 密度小, 熔点低
C.碱金属都导电、导热
D.钾的密度比钠大
某化学学习小组欲探究己烷的性质,用己烷进行下利实验:
实验1:

实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验3:根据下图的实验装置进行己烷催化裂化
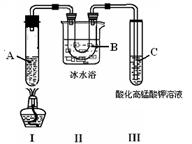
请回答下列问题:
(1)实验1中用到的玻璃仪器有(填名称) ;
(2)由实验1知己烷的物理性质有 ;
(3)实验2中的橙色溶液逐渐变浅的原因是 ;
A.己烷与溴发生发生取代反应 B.溴代己烷为无色物质
C.液溴向外挥发浓度降低 D.己烷与液溴发生加成反应
E.液溴与己烷分层,密度大的液溴在下层
(4)实验3的装置Ⅱ的作用是 ;
(5)试管C中看到的现象是 ,说明有 生成;
(6)试写出装置Ⅰ中发生有丙烷生成的裂化反应方程式:
。
某化学学习小组欲探究己烷的性质,用己烷进行下利实验:
实验1: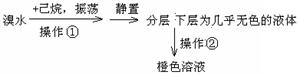
实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验3:根据下图的实验装置进行己烷催化裂化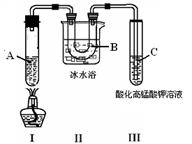
请回答下列问题:
(1)实验1中用到的玻璃仪器有(填名称) ;
(2)由实验1知己烷的物理性质有 ;
(3)实验2中的橙色溶液逐渐变浅的原因是 ;
| A.己烷与溴发生发生取代反应 | B.溴代己烷为无色物质 |
| C.液溴向外挥发浓度降低 | D.己烷与液溴发生加成反应 |
某化学学习小组欲探究己烷的性质,用己烷进行下利实验:
 实验1:
实验1:
 实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
实验3:根据右图的实验装置进行己烷催化裂化
请回答下列问题:
(1)实验1中用到的玻璃仪器有(填名称) ;
(2)由实验1知己烷的物理性质有 ;
(3)实验2中的橙色溶液逐渐变浅的原因是 ;
A.己烷与溴发生发生取代反应 B.溴代己烷为无色物质
C.液溴向外挥发浓度降低 D.己烷与液溴发生加成反应
E.液溴与己烷分层,密度大的液溴在下层
(4)实验3的装置Ⅱ的作用是 ;
(5)试管C中看到的现象是 ,说明有 生成;
(6)试写出装置Ⅰ中发生有丙烷生成的裂化反应方程式:
。
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取的主要原料.某化学学习小组对黄铁矿石进行如下实验探究:
[实验一]为测定硫元素的含量
Ⅰ.将m,g该黄铁矿样品放入如图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.
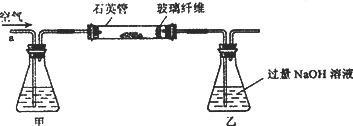
Ⅱ.反应结束后,将乙瓶中的溶液进行如图处理.
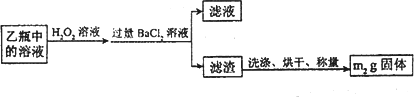
[实验二]测定铁元素的含量.Ⅲ.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解石英管中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250 mL;
④每次取稀释液25.00 mL,用已知物质的量浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL(该反应中还原产物为Mn2+)
请完成下列填空:
(1)已知12 g FeS2完全燃烧放热85.3 kJ,则FeS2燃烧热的化学方程式是________.
(2)Ⅰ中,甲瓶内所盛试剂是________溶液;乙瓶内发生反应的离子方程式有________;Ⅱ中玻璃纤维的作用是________.
(3)Ⅱ中,所加H2O2溶液需足量的理由是________.
(4)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还有________;
(5)该黄铁矿中硫元素的质量分数________(用Ⅰ、Ⅱ中有关实验数据表达);该黄铁矿中铁的元素的质量分数________(用Ⅰ、Ⅱ中有关实验数据表达)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com