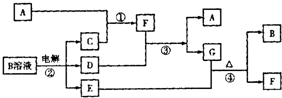
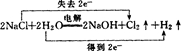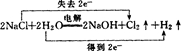(2012?青浦区二模)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).

| 实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
| 1 |
40mL HCl |
40mL NH3 |
产生白烟 |
| 2 |
40mL Cl2 |
10mL水 |
剩余气体为20mL |
| 3 |
30mL NO |
15mL O2 |
|
| 4 |
20mL AlCl3溶液 |
10mL NaOH溶液 |
生成白色沉淀,后消失 |
(1)如果实验1甲针筒内改装15mL Cl
2,乙针筒内仍为40mL NH
3,实验时,甲针筒内也有白烟产生.写出有关反应的化学方程式
3Cl2+8NH3=N2+6NH4Cl
3Cl2+8NH3=N2+6NH4Cl
.
(2)由实验2可知,常温常压下氯气在水中的溶解度为
1:2
1:2
.
(3)实验3反应后甲针筒内气体的体积为
15ml~30ml
15ml~30ml
.
(4)实验4中,AlCl
3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为
0.8
0.8
mol/L.
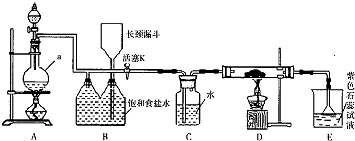
(5)将上述装置作以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如下图.在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体.将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半.A处的物质是
Na2O2
Na2O2
,甲针筒内的气体为
O2
O2
.

(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出).乙针筒内装有50mL空气.实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL.
(1)A处的物质是
c
c
(选填编号).
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
(2)已知空气中氧气的体积分数为0.2,则该实验的相对误差为
-0.05或-5%
-0.05或-5%
.