
题目列表(包括答案和解析)
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。请回答下列问题:
(1)S、N、O的第一电离能由大到小的顺序为 。
(2)血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
①写出亚铁离子的基态电子排布式 。
②CO可以和很多过渡金属形成配合物。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO中中心原子的杂化类型为 杂化,CO有多种等电子体,其中常见的两种为 。
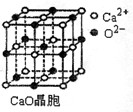
(3)SO2是一种大气污染物,为减轻SO2污染,火力发电厂生产中 常在燃煤中加入CaO以“固硫”。CaO晶胞如图所示,其中Ca2+的配位数为 ,CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO—3 401kJ/mol、NaCl—786kJ/mol。CaO晶体的熔点 NaCl晶体的熔点(填“高于”、“等于”或“低于”)。
(4)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是-19.5℃),甲醛是“假酒”中的主要有害物质(其沸点是64.65℃),1mol甲醛分子中![]() 键的数目为 ,甲醇的沸点明显高于甲醛的主要原因是 。
键的数目为 ,甲醇的沸点明显高于甲醛的主要原因是 。
1.《有机化学基础》
已知:两个羟基同时连在同一碳原子上的结构是不稳定的,它将发生脱水反应:
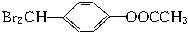
现有分子式为C9H8O2Br2的物质M,有机物C的相对分子质量为60,在一定条件下可发生下述一系列反应:
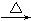
请回答下列问题:
(1)G→H的反应类型是_______________。
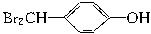
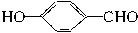
(2)M的结构简式为_______________;C的结构简式为_______________。
(3)写出下列反应的化学方程式:
①A→B的化学方程式:________________________________________________________;
②H→I的化学方程式:_________________________________________________________。
2.《物质结构与性质》Ⅰ.图表法、图像法是常用的科学研究方法。
图A 图B
(1)短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第_____族。
(2)图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第_____族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是_____(填“a”或“b”)。
Ⅱ.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为是钛(22Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(3)Ti元素的基态原子的价电子层排布式为____________。
(4)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定;偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如下图,它的化学式是__________;晶体内与每个“Ti”紧邻的氧原子数为_________个。
(5)已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() 。则绿色晶体配合物的化学式为_______________。
。则绿色晶体配合物的化学式为_______________。
阅读下列一段材料,并回答:
据《中国青年报》2002年9月20日报道:通过全球几十位科学家的通力合作,欧洲核子研究中心(CERN)成功地制造出约5万个反氢原子.这是人类首次在受控条件下大批量制造反物质.
反物质就是由反粒子构成的物质.所有的粒子都有反粒子.这些反粒子的特点是其质量、寿命、自旋、同位旋与相应的粒子相同,但电荷、重子数、轻子数等量子数与之相反.例如,氢原子由一个带负电的电子和一个带写上电的质子构成;反氢原子则与它正好相反,由一个带正电的反电子和一个带负电的反南子构成.物质与反物质的相遇后会湮灭,并释放出在量能量.
科学家认为,能够大量地制造反氢原子,对准确比较物质与反物质的差别,解答宇宙构成等问题将有重要意义.
(1)反氢原子的结构示意图中,正确的是
[ ]
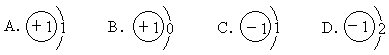
(2)如果制取了反氧原子,则下列说法中正确的是
[ ]
A.核内有8个带正电的质子,核外有8个带负电的电子
B.核内有8个带负电的电子,核外有8个带正电的质子
C.核内有8个带负电的中子,核外有8个带正电的质子
D.核内有8个带负电的质子,核外有8个带正电的电子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com